
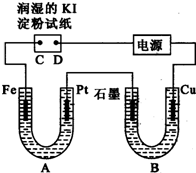
 ���װ����ͼ��ʾ��ͼ��Bװ��ʢ1L 3mol?L-1 K2SO4��Һ��Aװ����ʢ1L 3mol?L-1 AgNO3��Һ��ͨ��һ��ʱ�����ʪ�ĵ���KI��ֽ��C�˱���ɫ���Իش�
���װ����ͼ��ʾ��ͼ��Bװ��ʢ1L 3mol?L-1 K2SO4��Һ��Aװ����ʢ1L 3mol?L-1 AgNO3��Һ��ͨ��һ��ʱ�����ʪ�ĵ���KI��ֽ��C�˱���ɫ���Իش�| ������ | �״� | ��������� | |
| �۵�/�� | 122.4 | -97 | -12.3 |
| �е�/�� | 249 | 64.3 | 199.6 |
| �ܶ�/g?cm-3 | 1.2659 | 0.792 | 1.0888 |
| ˮ���� | �� | ���� | ���� |
| ||
| ||
| 1 |
| 3 |
| 0.0056L |
| 22.4L/mol |
| 0.001mol |
| 1L |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������� |
| B������������ |
| C���������������� |
| D���Զ��ױ��ͱ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
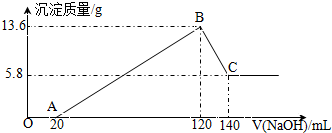 ��һ��������Mg-Al�Ͻ�Ͷ��100mLһ�����ʵ���Ũ�ȵ�ijHCl��Һ�У���ַ�Ӧ����Ӧ�����Һ����μ���һ�����ʵ���Ũ�ȵ�NaOH��Һ�����ɳ���������������NaOH��Һ�������ϵ��ͼ���ش��������⣺
��һ��������Mg-Al�Ͻ�Ͷ��100mLһ�����ʵ���Ũ�ȵ�ijHCl��Һ�У���ַ�Ӧ����Ӧ�����Һ����μ���һ�����ʵ���Ũ�ȵ�NaOH��Һ�����ɳ���������������NaOH��Һ�������ϵ��ͼ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
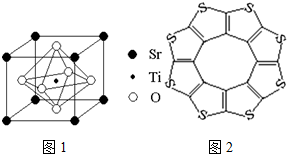 ������һ�ֽྻ�Ŀ�������Դ���Ʊ��ʹ������������ܿ����������ؼ����ڣ�
������һ�ֽྻ�Ŀ�������Դ���Ʊ��ʹ������������ܿ����������ؼ����ڣ�| C-S | C=S | C16S8��̼��� | |
| ����/pm | 181 | 155 | 176 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800�� | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800�� | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800�� | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800�� | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com