
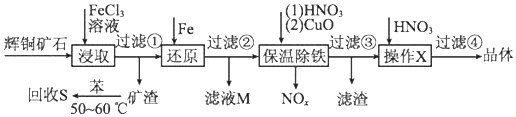
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
分析 辉铜矿加入氯化铁溶液溶解浸取过滤,发生反应Cu2S+4Fe3+=2Cu2++4Fe2++S,得到矿渣加入苯水浴加热回收硫单质;加入在滤液中加入铁还原铁离子和铜离子过滤,滤液M主要含有亚铁离子,滤保温除铁加入稀硝酸溶液和氧化铜反应,调节溶液pH除去杂质离子,过滤得到滤液为硝酸铜溶液,在稀硝酸溶液中蒸发浓缩,冷却结晶过滤洗涤得到晶体;
(1)铁离子做氧化剂被还原为亚铁离子,Cu2S被氧化,生成铜离子和硫单质;
(2)苯沸点比较低,温度过高苯容易挥发,温度过低溶解速率小;
(3)加入CuO调节溶液的PH,促进铁离子水解为氢氧化铁沉淀;
(4)得到晶体的方法是蒸发浓缩溶液,冷却结晶,据此解答即可.
解答 解:(1)铁具有还原性,铁离子、铜离子具有氧化性,均可以与金属铁反应被还原,反应的离子反应方程式分别为:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Cu+Fe2+;
故答案为:Fe+2Fe3+=3Fe2+;Fe+Cu2+=Cu+Fe2+;
(2)苯沸点比较低,温度过高苯容易挥发,温度过低溶解速率小;
故答案为:温度高苯容易挥发;温度低溶解速率小;
(3)铁离子水解:Fe3++3H2O?Fe(OH)3+3H+,加入CuO使水解平衡正向进行,调节溶液的PH使铁元素完全转化为氢氧化铁沉淀,
故答案为:调节溶液的pH,使Fe3+完全转化为Fe(OH)3沉淀;
(4)得到晶体的方法是蒸发浓缩溶液,冷却结晶;
故答案为:蒸发浓缩;冷却结晶.
点评 本题考查了物质分离提纯的方法和流程判断,主要是物质性质的理解应用和实验基本操作,掌握基础是关键,题目难度中等.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:选择题
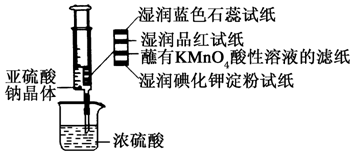 如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )| A. | 湿润的蓝色石蕊试纸先变红后褪色 | |
| B. | 湿润的品红试纸,蘸有KMnO4酸性溶液的滤纸均褪色证明了SO2的漂白性 | |
| C. | 湿润的碘化钾淀粉试纸未变蓝说明SO2氧化性强于I2 | |
| D. | 实验后,可把注射器中的物质推入NaOH溶液,以减少环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 冰水混合物 | CuSO4•5H2O | 液态 KNO3 | 蔗糖 |
| B | CaO溶液 | 海水 | 铜 | 酒精 |
| C | 氯气 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | Na2SO4溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蔗糖溶液不能导电,故蔗糖溶液时非电解质 | |
| B. | AgCl难溶于水,属于电解质 | |
| C. | SO3溶于水形成的溶液能导电,所以SO3是电解质 | |
| D. | 纯水的导电性很差,所以水不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O3 | C. | CuO | D. | Cu2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
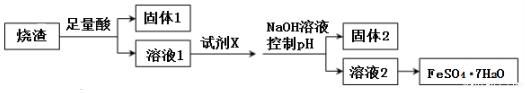
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
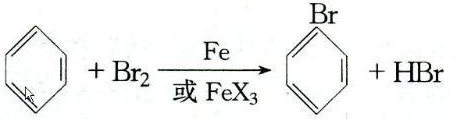 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠密封保存在水中 | |
| B. | 新制的氯水通常保存在无色试剂瓶中 | |
| C. | 氢氧化钠溶液保存在有玻璃塞的玻璃试剂瓶中 | |
| D. | 氢氟酸保存在塑料瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com