
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A. 高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B. 室温下,1 L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
【答案】D
【解析】试题分析:A.高温下,Fe与水蒸气反应生成四氧化三铁,四氧化三铁中Fe的化合价为![]() 价,因此Fe失去电子的物质的量为:
价,因此Fe失去电子的物质的量为:![]() ,根据得失电子守恒,生成H2的物质的量为:
,根据得失电子守恒,生成H2的物质的量为: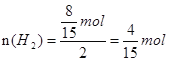 ,因此生成的H2分子数目为
,因此生成的H2分子数目为![]() ,A错误;B. 室温下,1 LpH=13的NaOH溶液中H+浓度为c(H+)=10-13mol/L,且H+全部由水电离,由水电离的OH-浓度等于水电离出的H+浓度,因此由水电离的OH-为10-13mol/L×1L=10-13mol,B错误;C. 氢氧燃料电池正极上氧气发生得电子的还原反应,当消耗标准状况下22.4L气体时,电路中通过的电子的数目为
,A错误;B. 室温下,1 LpH=13的NaOH溶液中H+浓度为c(H+)=10-13mol/L,且H+全部由水电离,由水电离的OH-浓度等于水电离出的H+浓度,因此由水电离的OH-为10-13mol/L×1L=10-13mol,B错误;C. 氢氧燃料电池正极上氧气发生得电子的还原反应,当消耗标准状况下22.4L气体时,电路中通过的电子的数目为![]() ,C错误;D.该反应中,生成28 g N2时,转移的电子数目为3.75NA,D正确。故答案D。
,C错误;D.该反应中,生成28 g N2时,转移的电子数目为3.75NA,D正确。故答案D。


科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH-COOH和油酸(C17H33COOH) B、C60和石墨 C、35Cl和37Cl
D、 E、乙醇和乙二醇
E、乙醇和乙二醇
①互为同位素的是______________;②互为同系物的是____________;
③互为同素异形体的是_____________;④互为同分异构体的是______________;
⑤既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是__________。
(2)选择合适的药品鉴别下列有机物组合(将试剂名称或者化学式填在横线上)
① CCl4和苯_____________ ②己烷和己烯_____________ ③苯和甲苯______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷与氯气以物质的量之比1∶3混合,在光照下得到的产物:①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4,正确的是 ( )
A、只有① B、只有②
C、①②③的混合物 D、①②③④的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/cm ,沸点约55℃,分离水和丙酮时最合理的方法是
A. 蒸馏 B. 分液 C. 过滤 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断开1molH﹣H键吸收的能量为436KJ,形成1molH﹣H键放出的能量为391KJ,根据化学方程式N2+3H2 ![]() 2NH3 , 反应完1molN2放出的能量为924KJ,则断开1molN=N键吸收的能量是( )
2NH3 , 反应完1molN2放出的能量为924KJ,则断开1molN=N键吸收的能量是( )
A.431KJ
B.649KJ
C.869KJ
D.945.6KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的性质决定物质反应的现象,关于钠与水反应的现象和钠的下列性质无关的是( )
A. 钠的熔点较低 B. 钠的密度小于水
C. 钠的硬度较小 D. 钠的还原性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 28g氮气所含有的原子数目为NA
B. 化学反应中1mol金属镁变成镁离子时失去电子数目为2NA
C. 标准状况下,22.4L水中含有个水分子NA
D. 标准状况下,22.4L氯化氢所含的原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油气“芳构化”是由石油气生产高辛烷值汽油的一种有效生产工艺。测得反应2C4H10![]() C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:
温度(℃) | 400 | 450 | 500 |
平衡常数K | a | 6a | 40a |
(1)该反应的正反应是________(填“吸热”或“放热”)反应。
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为____________________。
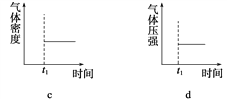
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是__________。

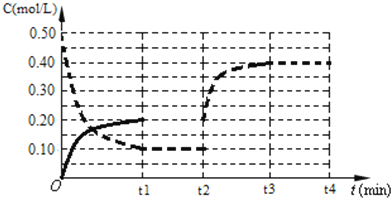
(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com