
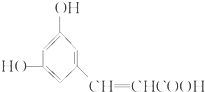
| A. | X分子中最多可有9个碳原子共平面 | |
| B. | X可以发生取代、加成、消去、聚合等反应 | |
| C. | 1 mol X与足量NaHCO3溶液反应所得物质的分子式为C9H7O4Na | |
| D. | 苯环上的取代基与X完全相同的X的同分异构体有5种 |
分析 该分子中含有苯环、酚羟基、碳碳双键、羧基,具有苯、酚、烯烃和羧酸的性质,能发生加成反应、取代反应、氧化反应、加聚反应、酯化反应等,据此分析解答.
解答 解:A.苯环中所用碳原子共平面,与C=C键连接的C原子共平面,则X分子中最多可有9个碳原子共平面,故A正确;
B.不能发生消去反应,故B错误;
C.只有-COOH可与碳酸氢钠反应,则1 mol X与足量NaHCO3溶液反应所得物质的化学式为 C9H7O4Na,故C正确;
D.对应的含有相同基团的同分异构体中,官能团可能的位置如图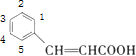 ,如固定-CH=CH-COOH,则两个-OH可有1、2;1、3;1、4;1、5;2、3;2、4等6种不同的位置,则对应的同分异构体有5种,故D正确;
,如固定-CH=CH-COOH,则两个-OH可有1、2;1、3;1、4;1、5;2、3;2、4等6种不同的位置,则对应的同分异构体有5种,故D正确;
故选B.
点评 本题考查有机物结构和性质,明确官能团及其性质关系即可解答,侧重考查苯、酚、烯烃和羧酸的性质,难点是碳原子共面个数及同分异构体种类判断,易错选项是D.


 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:选择题
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 1H和2H是不同的核素,它们的质子数相同 | |
| C. | 14C和14N的质量数相同,它们的中子数不等 | |
| D. | 6Li和7Li电子数相同,中子数也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给容器消毒 | B. | 杀死果实周围的细菌,防止霉变 | ||
| C. | 延长果实或花朵的寿命 | D. | 催熟果实或花朵 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,可以证明该结论的实验是(用离子方程式表示)Cl2+S2-═2Cl-+S↓
,可以证明该结论的实验是(用离子方程式表示)Cl2+S2-═2Cl-+S↓查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一种锌锰干电池外壳的纸层包装印有如图所示的文字,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加人MnO2氧化吸收H2)
一种锌锰干电池外壳的纸层包装印有如图所示的文字,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加人MnO2氧化吸收H2)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-甲基-2-丁烯 | B. | 2,3-二甲基-1-丁烯 | ||
| C. | 3-甲基-1-丁烯 | D. | 2-甲基-1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl:718 |
| 二氧化硅:1710 | Rb:39 | HI:-51 | CsCl:645 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氯乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,然后加入AgNO3溶液 | |
| C. | 加入NaOH溶液,加热后酸化,然后加入AgNO3溶液 | |
| D. | 加入NaOH的乙醇溶液,然后加入AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com