
| A. | H+、NO3-、Fe2+、Na+ | B. | Ag+、NO3-、Cl-、K+ | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、OH- |
分析 具有还原性的离子与具有氧化性的离子,发生氧化还原反应,不能大量共存,以此来解答.
解答 解:A.H+、NO3-、Fe2+发生氧化还原反应,不能大量共存,故A选;
B.Ag+、Cl-结合生成沉淀,因复分解反应不能大量共存,故B不选;
C.Ba2+、SO42-结合生成沉淀,因复分解反应不能大量共存,故C不选;
D.Cu2+、OH-结合生成沉淀,NH4+、OH-结合生成弱电解质,因复分解反应不能大量共存,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、复分解反应的离子共存考查,注意习题的限制条件,题目难度不大.


科目:高中化学 来源: 题型:解答题
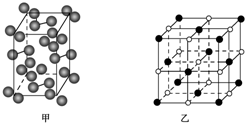
| 元素代号 | A | B | C |
| 第一电离能(kJ•mol-1) | 520 | 496 | 419 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种溶液的PH的大小是③>②>④>① | |
| B. | 若将4种溶液稀释相同的倍数,PH变化最大的是② | |
| C. | 若分别加入25 mL0.1 mol•L-1盐酸后,PH最大的是① | |
| D. | 若4种溶液的PH均为9,则物质的量浓度大小顺序是③>①>②>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的无色溶液中:Cl-、MnO4-、Ag+、SO42- | |
| B. | 在能使pH试纸变深蓝色的溶液中:Al3+、NO3-、S2-、CO32- | |
| C. | 在加入铝粉能产生H2的溶液中:NH4+、K+、SO42-、NO3- | |
| D. | 在由水电离出的c(OH-)=10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,AgCl在水中的溶解度大于在氯化钠溶液中的溶解度 | |
| B. | 浓FeCl3溶液滴入沸水加热形成红褐色透明液体 | |
| C. | 自然界地表层原生铜矿变成CuSO4溶液向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS) | |
| D. | 加入少量AgCl固体可以除去氯化钠溶液中的少量硫化钠杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v (NH3)=0.25 mol/(L•s) | B. | v (O2)=1.4mol/(L•min) | ||
| C. | v (H2O)=0.25 mol/(L•s) | D. | v (NO)=9 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物 | |
| B. | 油酸既能够使Br2的四氯化碳溶液褪色,也可使酸性KMnO4溶液褪色 | |
| C. | 蔗糖、麦芽糖的化学式都可表示为C12H22O11,二者互为同分异构体 | |
| D. | 向鸡蛋白溶液中加入饱和硫酸铵溶液析出白色沉淀,不属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com