
分析 (1)碳与浓硝酸在加热条件下反应生成二氧化碳、二氧化氮和水;
(2)高锰酸钾具有强的氧化性,能够氧化碳生成碳酸根离子、碳酸氢根离子,依据原子个数守恒、得失电子守恒书写反应的方程式;
(3)碳、一氧化碳具有还原性能够还原氧化铅,二氧化碳与炭在高温下反应生成一氧化碳.
解答 解:(1)碳与浓硝酸在加热条件下反应生成二氧化碳、二氧化氮和水,化学方程式:C+4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O;
故答案为:C+4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O;
(2)依据题意可知,锰元素由+7价降为+4价,C由0价升高为+4价,要使得失电子守恒,高锰酸钾根前系数为4,碳系数为3,依据原子个数守恒,反应方程式:4MnO4-+3C+H2O=4MnO2+2HCO3-+CO32-,
故答案为:4,3,1,4,2,HCO3-;
(3)碳、一氧化碳具有还原性能够还原氧化铅,二氧化碳与炭在高温下反应生成一氧化碳,反应的方程式:PbO+C$\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO↑ PbO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO2 CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO
2PbO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+CO2↑;
故答案为:PbO+C$\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO↑ PbO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Pb+CO2 CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO 2PbO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Pb+CO2↑.
点评 本题考查了化学方程式的书写,侧重考查氧化还原反应方程式书写,明确氧化还原反应得失电子守恒、原子个数守恒规律是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式: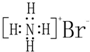 | |
| B. | S原子的结构示意图: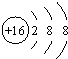 | |
| C. | 次氯酸的电子式: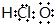 | |
| D. | 原子核内有18个中子的氯原子:${\;}_{17}^{35}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 14Si | 15P | 16S | 17Cl | |
| 单质与H2 反应的条件 | 高温 | 磷蒸气与 H2能反应 | 加热 | 光照或点燃 时发生爆炸 |
| 最高价氧化 物的水化物 | H4SiO4 弱酸 | H3PO4 中强酸 | H2SO4 强酸 | HClO4 最强含氧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国历史上铅的使用早于锌 | B. | 锌和铅有相似性但锌更活泼 | ||
| C. | 所得产品中混有煤炭 | D. | 属于热还原法冶炼金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释$\frac{c(O{H}^{-})}{c({H}^{+})}$增大的溶液:K+、Na+、SO42-、AlO2- | |
| B. | 常温下$\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3- | |
| C. | 铁片加入产生气泡的溶液:Na+、NH4+、I-、NO3- | |
| D. | NaHCO3溶液:K+、Na+、SO42-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素 | |
| B. | 根据相对分子质量的大小将共价化合物分为小分子化合物和高分子化合物 | |
| C. | 根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于2SO2(g)+O2(g)?2SO3(g)△H=QKJ/mol(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ | |
| B. | 热化学方程式中的化学计量数表示相应物质的物质的量,不能用分数表示 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 小苏打在水中的电离方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
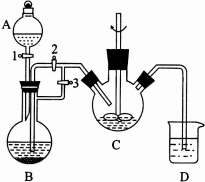 乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.
乳酸亚铁晶体([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是常用的补铁剂.乳酸亚铁可由乳酸与碳酸亚铁(易被空气中氧气氧化)反应制得:2CH3CH(OH)COOH+FeCO3→[CH3CH(OH)COO]2Fe+CO2↑+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com