
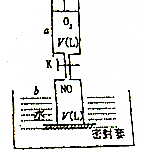
 如图所示,活塞的质量与筒壁的摩擦不计,与K相连的细管的体积也忽略不计,在标准状况下:
如图所示,活塞的质量与筒壁的摩擦不计,与K相连的细管的体积也忽略不计,在标准状况下:分析 (1)发生2NO+O2=2NO2,2NO2?N2O4,aL氧气参加反应气体体积减小;
(2)快速推a中活塞至a中气体全部进入b中,则压强增大,2NO2?N2O4正向移动;
(3)打开K,移走b的密封套,发生2H2O+4NO+3O2=4HNO3,以此计算.
解答 解:(1)发生2NO+O2=2NO2,2NO2?N2O4,aL氧气参加反应气体体积减小,
2NO+O2=2NO2 △V
1 1
V V
且发生2NO2?N2O4,为可逆反应,则$\frac{V}{2}$<△V(减小)<V,
故答案为:$\frac{V}{2}$<△V(减小)<V;
(2)快速推a中活塞至a中气体全部进入b中,则压强增大,2NO2?N2O4正向移动,则b中气体的颜色先变深后略变浅,是因体积缩小,气体密度变大,颜色加深,随后2NO2?N2O4平衡向右正向移动,NO2的浓度减小,
故答案为:b中气体的颜色先变深后略变浅;体积缩小,气体密度变大,颜色加深,随后2NO2?N2O4平衡向右正向移动,NO2的浓度减小;
(3)打开K,移走b的密封套,足够长时间发生2H2O+4NO+3O2=4HNO3,则观察到a、b中气体由无色逐渐变为红棕色,溶液(或水)缓慢进入b中,最终充满b,且a中充液约$\frac{3V}{4}$L,剩余气体为无色气体,反应后溶质为硝酸,由N原子守恒可知,硝酸的物质的量为$\frac{V}{22.4}$mol,溶液体积为(V+$\frac{3}{4}$V)L,则所得溶质的物质的量浓度为$\frac{\frac{V}{22.4}mol}{\frac{7}{4}L}$=0.255mol/L,故答案为:a、b中气体由无色逐渐变为红棕色,溶液(或水)缓慢进入b中,最终充满b,且a中充液约$\frac{3V}{4}$L,剩余气体为无色气体;0.255mol/L.
点评 本题考查化学实验方案的评价及实验装置的综合应用,为高频考点,把握发生的反应、平衡移动及物质的量浓度计算为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ①②③ | C. | ③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子.R+核外有28个电子.请回答下列问题(用所对应的元素符号表示).
已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子.R+核外有28个电子.请回答下列问题(用所对应的元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H6,C6H14,CCl4 | B. | C6H6,C2H5OH,CCl4 | ||
| C. | C6H6,C2H5OH,CH3COOC2H5 | D. | C6H5NO2,C2H5OH,CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{cV}{x}$×100% | B. | $\frac{cV}{25x}$×100% | C. | $\frac{40cV}{x}$×100% | D. | $\frac{cV}{4x}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断钠和镁的金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的NaOH溶液,判断镁与铝的金属性强弱 | |
| C. | 碳酸钠溶中滴加盐酸产生气泡,判断碳与氯的非金属性强弱 | |
| D. | F2与Cl2分别与足量的H2反应,判断氟与氯的非金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
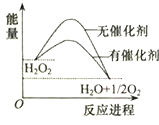
| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2→H2O+$\frac{1}{2}$O2+Q | |
| D. | 反应物的总能量高于生成物的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com