
(14分)高纯硅晶体是信息技术的重要材料。
(1)在周期表的以下区域中可以找到类似硅的半导体材料的是______(填字母)。
A.过渡元素区域 B.金属和非金属元素的分界线附近
(2)工业上用石英和焦炭可以制得粗硅。已知:
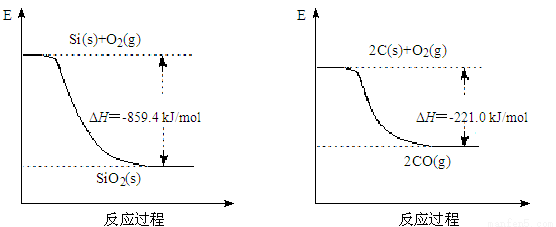
写出用石英和焦炭制取粗硅的热化学方程式 ______。
(3)某同学设计下列流程制备高纯硅:
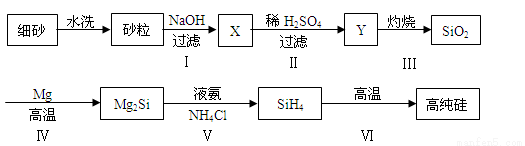
①Y的化学式为______。
②写出反应Ⅰ的离子方程式 。
③写出反应Ⅳ的化学方程式 。
④步骤Ⅵ中硅烷(SiH4)分解生成高纯硅,已知甲烷分解的温度远远高于硅烷,用原子结构解释其原因是 。
(4)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:
SiHCl3 (g) + H2(g)  Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是 (填字母)。
Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是 (填字母)。
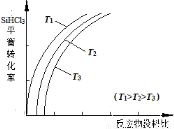
A.该反应是放热反应
B.横坐标表示的投料比应该是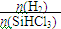
C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2014-2015学年北京市海淀区高三一模理综化学试卷(解析版) 题型:填空题
(14分)煤粉中的氮元素在使用过程中的转化关系如下图所示:
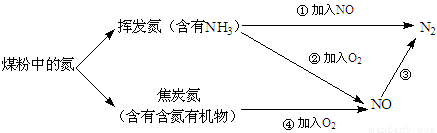
(1)②中NH3参与反应的化学方程式为 。
(2)③中加入的物质可以是 (填字母序号)。
a.空气 b.CO c.KNO3 d.NH3
(3)焦炭氮中有一种常见的含氮有机物吡啶(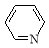 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更 (填“强”或“弱”),从原子结构角度解释原因: 。
),其分子中相邻的C和N原子相比,N原子吸引电子能力更 (填“强”或“弱”),从原子结构角度解释原因: 。
(4)已知:N2(g) + O2(g)===2NO(g) ΔH = a kJ·mol-1
N2(g) + 3H2(g)===2NH3(g) ΔH = b kJ·mol-1
2H2(g) + O2(g)===2H2O(l) ΔH = c kJ·mol-1
反应后恢复至常温常压,①中NH3参与反应的热化学方程式为 。
(5)用间接电化学法除去NO的过程,如下图所示:

已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式: 。
用离子方程式表示吸收池中除去NO的原理: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市西城区高三二模理综化学试卷(解析版) 题型:选择题
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是
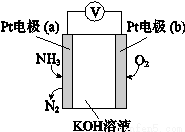
A.O2在电极b上发生还原反应
B.溶液中OH—向电极a移动
C.反应消耗的NH3与O2的物质的量之比为4:5
D.负极的电极反应式为:2NH3-6e—+6OH—=N2+6H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三4月模拟练习化学试卷(解析版) 题型:填空题
根据下列各组溶解度曲线图,判断分离提纯方法。
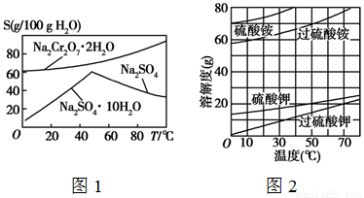
(1)根据图1中Na2SO4和Na2SO4·10H2O的溶解度曲线(g/100 g水),由Na2SO4溶液得到Na2SO4固体的操作为:将溶液升温结晶、 、用乙醇洗涤后干燥。用乙醇洗涤而不用水洗的原因是 。
(2)根据图2所示相关物质的溶解度曲线。在实验室中提纯过硫酸钾粗产品的实验具体操作依次为:将过硫酸钾粗产品溶于适量水中, ,干燥。
(3)根据图1中红矾钠(Na2Cr2O7·2H2O)和Na2SO4的溶解度曲线。从Na2Cr2O7和 Na2SO4的混合溶液中提取红矾钠的操作为:先将混合溶液蒸发浓缩,趁热过滤。趁热过滤的目的是 ;然后将滤液 ,从而析出红矾钠。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三4月模拟练习化学试卷(解析版) 题型:选择题
在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g) 4C(g)+D(g)ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g)ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是

A.若保持压强一定,当温度升高后,则图中θ>45°
B.若再加入B,则正、逆反应速率均逐渐增大
C.平衡时B的转化率为50%
D.若保持压强一定,再加入B,则平衡后反应体系气体密度减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三第二次模拟理综化学试卷(解析版) 题型:选择题
关于下列各装置图的叙述中,不正确的是
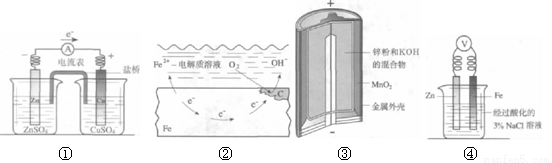
A.①中总反应为Zn + CuSO4 =Cu + ZnSO4
B.②中正极反应为2H2O + O 2 + 4e-=4OH-
C.③中负极反应为Zn+2OH-- 2e-=Zn(OH)2
D.④中向Fe电极区滴入2滴铁氰化钾溶液产生蓝色沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市五校高三第二学期联考化学试卷(解析版) 题型:实验题
(本题14分)
氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。

请回答下列问题:
(1).氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂______________________;
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板____________________________。
(2).吸收剂X的化学式为 ;氧化剂Y的化学式为________________。
(3).碱性条件下反应①的离子方程式为____________________________________。
(4).过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。该反应的化学方程式为
2KOH+Na2FeO4→K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因_________。
(5).K2FeO4 在水溶液中易发生反应:4FeO42+10H2O 4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
4Fe(OH)3+8OH+3O2↑。在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O B.稀KOH溶液、异丙醇
C.NH4Cl溶液、异丙醇 D.Fe(NO3)3溶液、异丙醇
(6).可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式为:
①FeO42-+CrO2-+2H2O→CrO42-+Fe(OH)3↓+OH-
②2CrO42-+2H+→Cr2O72-+H2O
③Cr2O72- +6Fe2++14H+→2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤,滤液定容于250 mL容量瓶中。每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。则上述样品中高铁酸钾的质量分数为 。(答案用小数表示,保留3位小数)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市五校高三第二学期联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列叙述正确的是
A.常温常压下,2.8 g N2与C2H4的混合气体中含有的电子数为1.4NA
B.标准状况下,1.12 L NO与1.12 L O2的混合物中含有的原子数为0.2NA
C.25 ℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氧原子数为0.3NA
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省太原市高二4月阶段形成检测化学试卷(解析版) 题型:填空题
(9分)当今世界,能源的发展日益成为全世界、全人类共同关心的问题。
(1)A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 |
A | 899 | 1 757 | 14 840 | 21 000 |
B | 738 | 1 451 | 7 733 | 10 540 |
①请根据上述信息,写出A的核外电子排布式:__________________。
②某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了________。
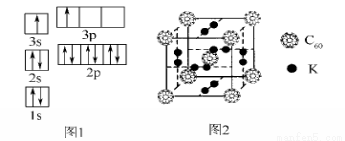
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中碳碳键的键长为154.45 pm,C60中碳碳键的键长为145 pm和140 pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由, 理由:_____________________。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体。该物质中K原子和C60分子的个数比为____________。
③继C60后,科学家又合成Si60、N60,请比较C、Si、N原子电负性由大到小的顺序 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则一个Si60分子中所含π键的数目为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com