

 .
.分析 A为淡黄色固,B是最常见的无色液体,A、B可以相互反应,则可推知A为Na2O2,B为H2O,二者反应生成氢氧化钠与氧气,E、G常见金属单质,L是一种易氧化的白色沉淀,由转化关系可知,G为Fe,E为Al,C为O2,D为NaOH,F为Fe3O4,H为Al2O3,I为NaAlO2,J为FeCl3,K为FeCl2,L为Fe(OH)2,据此答题.
解答 解:A为淡黄色固,B是最常见的无色液体,A、B可以相互反应,则可推知A为Na2O2,B为H2O,二者反应生成氢氧化钠与氧气,E、G常见金属单质,L是一种易氧化的白色沉淀,由转化关系可知,G为Fe,E为Al,C为O2,D为NaOH,F为Fe3O4,H为Al2O3,I为NaAlO2,J为FeCl3,K为FeCl2,L为Fe(OH)2.
(1)D为NaOH,NaOH中阴离子的电子式为 ,故答案为:
,故答案为: ;
;
(2)7.8g Na2O2 的物质的量为$\frac{7.8g}{78g/mol}$=0.1mol,可以生成0.2molNaOH,由2Al+2H2O+2NaOH=2NaAlO2+3H2↑,可知最多可制得NaAlO2的物质的量为0.2mol,故答案为:0.2mol;
(3)反应E+D→I的离子方程式:2Al+2H2O+2OH-=2AlO2-+3H2↑,故答案为:2Al+2H2O+2OH-=2AlO2-+3H2↑;
(4)L的悬浊液与C反应的化学方程式:4Fe(OH)2+2H2O+O2=4Fe(OH)3,故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3.
点评 本题考查无机物推断,涉及Fe、Al元素单质化合物性质,物质的颜色及转化中特殊反应等是推断突破口,需要学生熟练掌握基础知识,难度中等.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:填空题

| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH4 | CH3-CH3 | CH2═CH2 |
| 物质的量分数 | 20% | 30% | 50% |
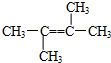 所示,
所示,查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3溶液$\stackrel{△}{→}$Fe2O3 | |
| B. | 饱和NaCl(aq) $\stackrel{先通NH_{3},再通CO_{2}}{→}$ NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | Al2O3$\stackrel{NaOH(aq)}{→}$NaAlO2(aq) $\stackrel{足量稀H_{2}SO_{4}}{→}$Al(OH)3 | |
| D. | 海水$\stackrel{Ca(OH)_{2}}{→}$Mg(OH)2$\stackrel{HCl(aq)}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子:12C | B. | HClO的结构式:H-Cl-O | ||
| C. | 镁离子的结构示意图: | D. | 乙酸的分子式:C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、NO3-、Cl- | B. | Ca2+、K+、Cl-、NO3- | ||
| C. | Al3+、K+、OH-、NO3- | D. | Na+、Ca2+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4晶体中阳离子和阴离子 | B. | Na2O2晶体中阴离子和阳离子 | ||
| C. | Mg2+离子中的质子和中子 | D. | 氯化钠中的质子总数和电子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COO-)<c(Na+) | B. | c(CH3COO-)>c(Na+) | C. | c(OH-)=c(CH3COO-) | D. | c(OH-)>c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com