
分析 (1)红热的铁跟水蒸气反应生成四氧化三铁和氢气;
(2)过氧化钠和二氧化碳反应生成碳酸钠和水;
(3)氯气与NaOH溶液反应生成NaCl、NaClO和水.
解答 解:(1)红热的铁跟水蒸气反应生成四氧化三铁和氢气,故化学方程为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故答案为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)过氧化钠和二氧化碳反应生成碳酸钠和氧气,该反应为2Na2O2+CO2═2Na2CO3+O2,故答案为:2Na2O2+CO2═2Na2CO3+O2;
(3)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O.
点评 本题考查化学反应方程式的书写,明确反应的条件及反应产物是解答的关键,并注意反应方程式的配平,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2在反应中被还原 | |
| B. | NaClO3在反应中失去电子 | |
| C. | H2SO4在反应中作氧化剂 | |
| D. | 1 mol氧化剂在反应中得到1 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
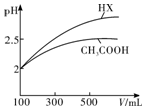
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡 常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15mol 20% | B. | 20mol 20% | C. | 20mol 80% | D. | 40mol 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用甘蔗生产的乙醇燃料属于可再生能源,利用乙醇燃料不会产生温室气体 | |
| B. | 低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,可减少雾霾的发生 | |
| C. | 太阳能、风能和生物能源属于新能源 | |
| D. | 太阳能电池可将太阳能直接转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 5:1 | C. | 3:13 | D. | 4:15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(C{l}^{-})}$<1 | |
| B. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$变大 | |
| C. | 将CH3COONa溶液加入水稀释后,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| D. | 向0.1 mol•L-1 CH3COOH溶液从20℃升温至30℃,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com