
| A. | 0.01mol/L CH3COOH溶液 | B. | 0.01mol/L HNO3溶液 | ||
| C. | pH=2的H2SO4溶液 | D. | pH=2的CH3COOH溶液 |
分析 在10mL 0.01mol/L的NaOH溶液中,氢氧化钠的物质的量为:n(NaOH)=0.01L×0.01mol/L=1×10-4mol;加入10mL某酸,再滴入紫色石蕊试液,溶液显红色,说明反应后溶液显示酸性,即酸过量;根据各选项的数据进行判断酸是否过量即可.
解答 解:氢氧化钠的物质的量为:n(NaOH)=0.01L×10-2mol/L=1×10-4mol,滴入紫色石蕊试液后溶液显红色,溶液显示酸性,说明酸过量,
A.10mL 0.01mol/L CH3COOH,醋酸的物质的量为:n(CH3COOH)=0.01L×10-2mol/L=1×10-4mol,等物质的量的氢氧化钠与醋酸反应恰好生成醋酸钠,醋酸根离子水解,溶液显示碱性,故A错误;
B.10mL 0.01mol/L HNO3,HNO3的物质的量为:n(HNO3)=0.01L×10-2mol/L=1×10-4mol,等物质的量的硝酸与氢氧化钠恰好反应生成硝酸钠,溶液显示中性,故B错误;
C.pH=2的H2SO4溶液中,氢离子浓度为0.01mol/L,硫酸为强电解质,10mL 该硫酸溶液中氢离子物质的量为:0.01L×10-2mol/L=1×10-4mol,硫酸与氢氧化钠恰好完全反应生成硫酸钠,溶液显示中性,故C错误;
D.pH=2的CH3COOH溶液,醋酸为弱电解质,溶液中醋酸的浓度大于0.0mol/L,醋酸的物质的量大于0.01L×10-2mol/L=1×10-4mol,醋酸溶液与氢氧化钠溶液反应后醋酸过量,溶液显示酸性,故D正确;
故选D.
点评 本题考查了酸碱溶液混合后溶液酸碱性判断,题目难度中等,注意明确弱电解质在溶液中部分电离,如选项D,pH=2的CH3COOH溶液,醋酸的物质的量浓度大于0.01mol/L;试题培养了学生的分析、理解能力及灵活应用所学知识的能力.


科目:高中化学 来源: 题型:实验题
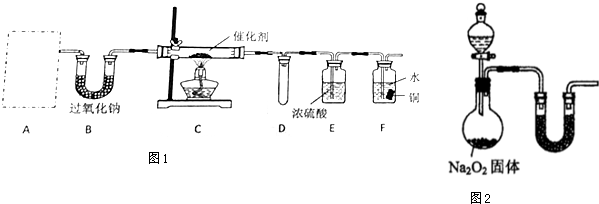
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氨水稀释后,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| B. | 0.1 mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 | |
| D. | 298 K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
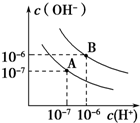 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
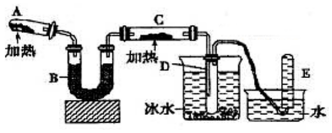 己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.
己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com