
| A.亚硝酸盐有强氧化性 |
| B.普通血红蛋白有较强氧化性 |
| C.亚硝酸盐中毒后,使用美蓝,高铁血红蛋白被还原 |
| D.中毒与解毒过程中都发生了氧化还原反应 |
 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源:不详 题型:单选题
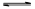 KI3
KI3| A.Na2S2O3 | B.AlCl3 | C.Na2CO3 | D.NaNO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.O3在反应中被氧化为O2 | B.1molO3在反应中得到6mol电子 |
| C.KI在反应中被还原为I2 | D.KI在反应中被氧化为I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应中硫元素被氧化,所有铁元素均被还原 |
| B.氧化剂是Fe3+,氧化产物是Cu2+ |
| C.反应中转移电子的物质的量为x mol |
| D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应的氧化产物仅为S |
| B.生成1molH3AsO2时。转移电子个数为10NA |
| C.将反应设计成一原电池,则NO2应该在正极附近逸出 |
| D.反应产生的NO2与56LO2混合在水中正好完全反应生成硝酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,找出其中一个变化与“
,找出其中一个变化与“ ”组成一个反应,写出该反应的离子方程式____ 。
”组成一个反应,写出该反应的离子方程式____ 。
 由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。
由此可知,高锰酸根离子(MnO—4)反应后的产物与 有关。

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AlN + 3CO↑
2AlN + 3CO↑| A.在氮化铝的合成反应中,N2是还原剂 |
| B.在氮化铝的合成反应中,C是还原剂 |
| C.氮化铝中氮元素的化合价为-3 |
| D.上述反应中每生成1molAlN,转移3 mol e- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com