
| A、NaHCO3溶液 |
| B、NaHSO4溶液 |
| C、Na2CO3溶液 |
| D、氨水与盐酸混合后c(NH4+)>c(Cl-)的溶液 |
科目:高中化学 来源: 题型:
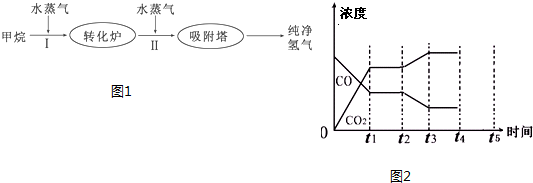
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
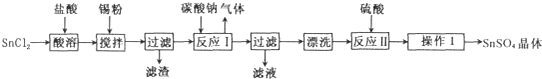
查看答案和解析>>
科目:高中化学 来源: 题型:
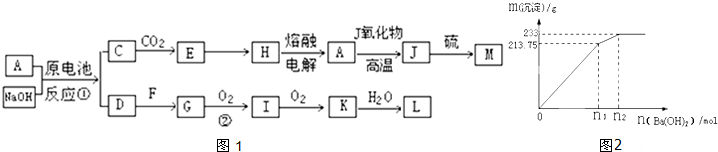
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=10的氨水稀释100倍 |
| B、pH=11的NaOH溶液与pH=5的盐酸等体积混合 |
| C、pH=8的NaOH溶液与pH=8的氨水等体积混合 |
| D、pH=4的醋酸和pH=10的NaOH溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、已知:
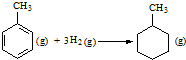 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| B、将足量SO2通入Ba(NO3)2溶液中有沉淀生成的离子方程式,3SO2+Ba2++2NO3-+2H2O=BaSO4↓+2NO+2SO42-+4H+ | ||||||||||
| C、电解稀硫酸不可能发生的反应:Cu+H2SO4=CuSO4+H2↑ | ||||||||||
| D、1000℃时,Na2SO4与H2发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g)△H>0,反应达到平衡后,将体系中的Na2S(s)全部移走,平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Fe3+有氧化性 | FeCl3溶液可溶解废旧电路板中的铜 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | NH3有还原性 | NH3可用H2SO4吸收 |
| D | 浓HNO3有酸性 | 浓HNO3不可用铁制容器盛放 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入一定量pH=2的醋酸,混合后所得的溶液中:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
| B、向其中加入一定量的水,NH3?H2O的电离平衡正移,溶液中所有离子浓度均减小 |
| C、与等体积、pH=2的盐酸混合后所得的溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(NH4+)+c(NH3?H2O)=1.0×10-12 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z简单离子的半径依次增大 |
| B、将M溶液加热蒸干并灼烧,最后可得Y的氧化物 |
| C、Y的最高价氧化物为碱性氧化物 |
| D、将少量X单质投入到M溶液中,会置换出Y单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com