
分析 (1)①PM2.5”是指大气层中直径≥2.5μm的颗粒物,能被肺吸收并进入血液,对人体危害很大,是形成雾霾的主要污染物;
②用厨余垃圾生产沼气 变废为宝;废旧塑料露天焚烧产生有毒有害气体,废旧电池中含有重金属,就地填埋会对水土造成严重污染;
③劣质胶合板释放的主要污染物是甲醛,释放后造成室内污染;
(2)①维生素C又称 抗坏血酸.维生素C具有还原性,受热更易被氧化,蔬菜生吃比熟吃时维生素C的损失小;
②每克脂肪在人体内氧化分解产生约为37.6kJ的热量,葡萄糖约为16.4kJ,蛋白质约为16.7kJ;葡萄糖在人体内发生氧化反应的化学方程式为:C6H12O6+6O2═6CO2+6H2O.
解答 解:(1)①导致雾霾形成的主要污染物是PM2.5,故答案为:c;
②用厨余垃圾生产沼气 变废为宝;废旧塑料露天焚烧产生有毒有害气体,废旧电池中含有重金属,就地填埋会对水土造成严重污染,故答案为:a;
③甲醛是劣质胶合板释放的主要污染物,造成室内污染,故答案为:c;
(2)①维生素C又称抗坏血酸.蔬菜生吃比熟吃时维生素C的损失小,原因是维生素C具有还原性,受热更易被氧化,故答案为:抗坏血;维生素C受热更易被氧化;
②每克脂肪在人体内氧化分解产生约为37.6kJ的热量,葡萄糖约为16.4kJ,蛋白质约为16.7kJ,等质量的上述物质提供能量最多的是油脂;葡萄糖在人体内发生氧化反应的化学方程式为:C6H12O6+6O2═6CO2+6H2O,故答案为:油脂;C6H12O6+6O2═6CO2+6H2O.
点评 本题主要考查了常见的污染物、营养与健康等知识,与生产生活密切相关,难度不大,注意知识的积累.


科目:高中化学 来源: 题型:解答题
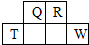 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题: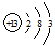 .
.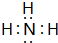
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
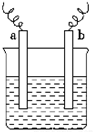 如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )
如图中,两电极上发生的电极反应如下:a极:Cu2++2e-═Cu;b极:Fe-2e-═Fe2+,则以下说法中不正确的是( )| A. | 该装置一定是原电池 | |
| B. | a极上一定发生还原反应 | |
| C. | a、b可以是同种电极材料 | |
| D. | 该过程中能量的转换可以是电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成2n mol X,同时消耗nmol Y | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度相等 | |
| D. | 容器内气体的压强不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
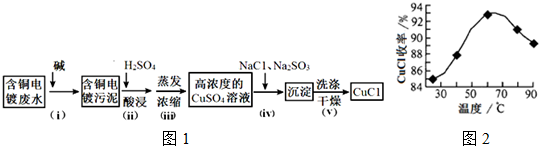
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
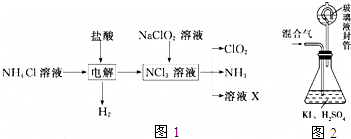
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com