
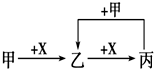
 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合如图.则甲和X(要求甲和X能互换)不可能是[提示:Al3++3AlO2-+6H2O=4Al(OH)3↓]( )| A、C和O2 |
| B、SO2和NaOH溶液 |
| C、Cl2和Fe |
| D、AlCl3溶液和NaOH溶液 |
| O2 |
| O2 |
| C |
| C |
| C |
| O2 |
| NaOH |
| NaOH |
| SO2 |
| SO2 |
| SO2 |
| NaOH |
| Fe |
| Fe |
| Cl2 |
| Cl2 |
| NaOH |
| NaOH |
| AlCl3 |
| AlCl3 |
| AlCl3 |
| NaOH |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| A、受热后的蒸发皿要用坩埚钳夹取,并放在石棉网上冷却 |
| B、稀释浓硫酸时,应在量筒中先加入一定量水,再沿器壁缓慢注入浓硫酸,并用玻璃棒搅拌 |
| C、过滤时,为了加速溶液透过滤纸,可以用玻璃棒末端轻轻搅拌滤纸上的混合物 |
| D、分液时,先将分液漏斗下层液体从下口放出,然后换一个烧杯再从下口放出上层液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
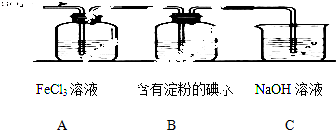
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用酒精作萃取剂提取碘水中的碘 |
| B、用分液的方法分离溴和四氯化碳 |
| C、用蒸馏的方法除去水中的Na+离子 |
| D、用过滤的方法除去水中的泥沙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:8 |
| C、1:4 | D、1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
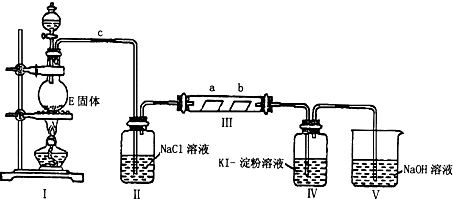
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ |
| 0.1mol/L NaOH溶液 | pH=11 NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH=3 CH3COOH溶液 |
| A、由水电离出的c(H+):③<① |
| B、③稀释到原来的100倍后,pH与④相同 |
| C、①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH) |
| D、②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为:c(CH3COOˉ)>c(H+)>c(Na+)>c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸和氢氧化钠溶液之间的中和反应 | ||||
B、CO2+C
| ||||
C、金属镁燃烧:2Mg+O2
| ||||
| D、生石灰溶于水:CaO+H2O=Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com