
【题目】某小组研究溶液中Fe2+与![]() 、
、![]() 的反应。
的反应。
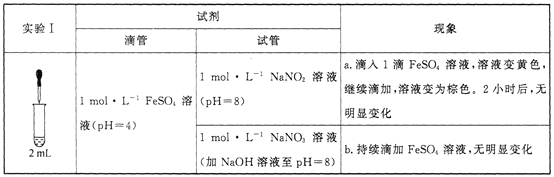
已知:[Fe(NO)]2+在溶液中呈棕色。
(1)研究现象a中的黄色溶液。
①用__________溶液检出溶液中含有Fe3+。
②甲认为是O2氧化了溶液中的Fe2+。乙认为O2不是主要原因,理由是_____________。
③进行实验Ⅱ,装置如图所示。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。产生NO的电极反应式为_______实验Ⅱ的目的是________。
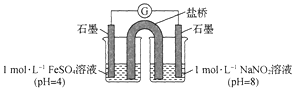
(2)研究现象a中的棕色溶液。综合实验I和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的Fe2+或Fe3+发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为Fe2+与NO发生了反应。实验Ⅲ的操作和现象是_______。
(3)研究酸性条件下,溶液中Fe2+与![]() 、
、![]() 的反应。
的反应。
序号 | 操作 | 现象 |
i | 取1 mol·L-l的NaNO2溶液,加稀硫酸至pH = 3,加入1 mol·L-l FeSO4溶液 | 溶液立即变为棕色 |
ii | 取1 mol·L-l的NaNO3溶液,加硫酸至pH = 3,加入1 mol·L-l FeSO4溶液 | 无明显变化 |
iii | 分别取0.5 mL l mol·L-l的NaNO3溶液与1 mol·L-l的FeSO4溶液,混合,小心加入0.5 mL浓硫酸 | 液体分为两层,稍后,在两层液体界面上出现棕色环 |
i中溶液变为棕色的离子方程式为_______、__________。
实验结论:本实验条件下,溶液中![]() 、
、![]() 的氧化性与溶液的酸碱性等有关。
的氧化性与溶液的酸碱性等有关。
【答案】KSCN 两个实验过程均有O2但NaNO3溶液中无明显变化 ![]() +e-+H2O === NO↑+2OH- 证实Fe2+被
+e-+H2O === NO↑+2OH- 证实Fe2+被![]() 氧化生成Fe3+ 将NO通入FeSO4溶液中溶液由浅绿色变黄色最后变棕色,将NO通入Fe2(SO4)3溶液中,无明显变化 Fe2++
氧化生成Fe3+ 将NO通入FeSO4溶液中溶液由浅绿色变黄色最后变棕色,将NO通入Fe2(SO4)3溶液中,无明显变化 Fe2++![]() +2H+=== Fe3++NO↑+H2O Fe2++NO === [Fe(NO)]2+
+2H+=== Fe3++NO↑+H2O Fe2++NO === [Fe(NO)]2+
【解析】
(1)①可用![]() 检验铁离子;
检验铁离子;
②对比实验中滴加溶液都会携带氧气;
③![]() 在正极上得电子被还原生成
在正极上得电子被还原生成![]() ,可证明
,可证明![]() 与亚铁离子发生氧化还原反应;
与亚铁离子发生氧化还原反应;
(2)要证明![]() 与
与![]() 发生了反应,可将
发生了反应,可将![]() 分别通入
分别通入![]() 溶液中,根据颜色变化判断;
溶液中,根据颜色变化判断;
(3)酸性条件下,![]() 溶液、
溶液、![]() 溶液发生氧化还原反应生成
溶液发生氧化还原反应生成![]() ,亚铁离子与
,亚铁离子与![]() 反应生成
反应生成![]() 。
。
(1)①KSCN与铁离子反应,溶液显血红色,则可用![]() 检验铁离子,
检验铁离子,
故答案为:![]() ;
;
②对比实验中滴加溶液都会携带氧气,但![]() 溶液中无明显变化,则
溶液中无明显变化,则![]() 不是主要原因,
不是主要原因,
故答案为:两个实验过程均有![]() ,但
,但![]() 溶液中无明显变化;
溶液中无明显变化;
③![]() 在正极上得电子被还原生成
在正极上得电子被还原生成![]() ,电极方程式为
,电极方程式为![]() ,实验Ⅱ的目的是证实
,实验Ⅱ的目的是证实![]() 被
被![]() 氧化生成
氧化生成![]() ,
,
故答案为:![]() ;证实
;证实![]() 被
被![]() 氧化生成
氧化生成![]() ;
;
(2)想证明![]() 与
与![]() 发生了反应,可将
发生了反应,可将![]() 分别通入
分别通入![]() 溶液中,可观察到将
溶液中,可观察到将![]() 通入
通入![]() 溶液中,溶液由浅绿色变黄色最后变棕色,将
溶液中,溶液由浅绿色变黄色最后变棕色,将![]() 通入
通入![]() 溶液中,无明显变化,
溶液中,无明显变化,
故答案为:将![]() 通入
通入![]() 溶液中,溶液由浅绿色变黄色最后变棕色,将
溶液中,溶液由浅绿色变黄色最后变棕色,将![]() 通入
通入![]() 溶液中,无明显变化;
溶液中,无明显变化;
(3)酸性条件下,![]() 溶液、
溶液、![]() 溶液发生氧化还原反应生成
溶液发生氧化还原反应生成![]() ,亚铁离子与
,亚铁离子与![]() 反应生成
反应生成![]() ,反应的离子方程式为
,反应的离子方程式为![]() ,同时发生
,同时发生![]() ,
,
故答案为:![]() ;
;![]() 。
。


科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如图:
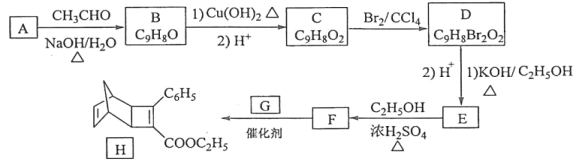
已知:
①RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
②![]()
回答下列问题:
(1)A的化学名称是___。
(2)由C生成D和E生成F的反应类型分别是__、__。
(3)E的结构简式为___。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为__。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出2种符合要求的X的结构简式__、__。
(6)写出用环戊烷和2–丁炔为原料制备化合物 的合成路线__(其他试剂任选)。
的合成路线__(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子中,各分子的立体构型和中心原子的杂化方式均正确的是( )
A. NH3 平面三角形 sp3杂化 B. CCl4 正四面体 sp3杂化
C. H2O V形 sp2杂化 D. CO32﹣ 三角锥形 sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是

A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖由约翰·B·古迪纳夫、M·斯坦利·威廷汉、吉野彰三人分获,以表彰他们研究锂离子电池做出的贡献。锂离子正极材料有LiMO2(M=Co、Ni、Mn) .
回答下列问题:
(1)基态Co原子价电子排布式为______,基态Li原子核外电子运动状态有____种。
(2)锂离子电池电解常用的锂盐有LiClO4、LiBF4等,常采用有机溶剂有乙醚、丙烯酯(![]() )等。
)等。
①LiClO4中阴离子空间构型为______,与其键合方式相同、空间构型也相同的离子和分子是___________________________ (各举一例).
②Li、Cl、F、B的电负性从大到小的顺序为_____;丙烯碳酸酯中碳原子的杂化方式是____。
③C2H5OC2H5(乙醚)的沸点比乙醇的低,其原因是________________。
(3)LiCoO2的晶胞是六棱柱,其结构如图所示:

晶胞中含氧原子数为_____,若晶胞的底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,则LiCoO2的密度为_______g·cm —3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 向水中通入氯气:Cl2+H2O===2H+ + ClO+ Cl
B. 向Ca(HCO3)2溶液中滴加足量NaOH溶液:Ca2+ + 2HCO3+2OH===CaCO3↓+CO32+2H2O
C. 向明矾溶液中加过量氨水:Al3++4NH3·H2O===AlO2+4NH4++2H2O
D. 将Fe2O3溶解与足量HI溶液:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
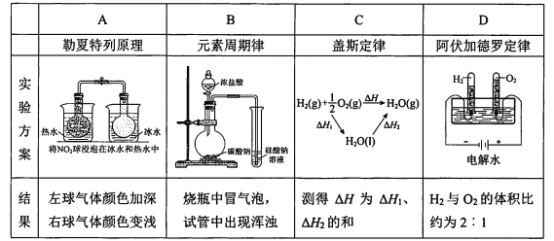
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某苯的衍生物,含有两个互为对位的取代基,其分子式为C8H10O,其中不溶解于NaOH溶液的该衍生物的结构式有( )
A.1种B.2种C.3种D.4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件。该小组同学为探究中毒原因进行了如下实验。
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO-具有氧化性。实验如下:
Ⅰ. 用pH试纸检验,漂白液pH>7,饱和![]() 溶液pH<7。
溶液pH<7。
Ⅱ. 取10 mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸。
Ⅲ. 另取10 mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色。
Ⅳ. 再取10 mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色。
①漂白液pH大于7的原因是(用离子方程式表示)__________。
②由实验Ⅱ得出ClO-具有氧化性,写出相应的离子方程式__________。
③对比实验Ⅲ和Ⅳ说明ClO-氧化性与溶液酸碱性的关系是__________。
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成。用图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2。

①装置B的作用是__________;盛放的药品是__________。
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生。A中反应的离子方程式________。
③若打开分液漏斗活塞向烧瓶中加入饱和![]() 溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加
溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加![]() 溶液反应的离子方程式是__________。
溶液反应的离子方程式是__________。
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2。若取10 mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com