
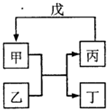
 甲乙丙丁戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足右图转化关系的是( )
甲乙丙丁戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各物质中,不满足右图转化关系的是( ) | 甲 | 乙 | 丙 | 戊 | |
| A | NH3 | Cl2 | N2 | H2 |
| B | C | SiO2 | CO | CuO |
| C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | CO2 |
| D | 乙醇乙酯 | NaOH溶液 | 乙醇 | 乙酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据反应甲+乙→丙+丁,丙+戊→甲分析,将四个选项中的各物质代入,结合物质的性质判断这两个反应是否能发生,如果能发生,则正确,否则错误.
解答 解:A.8NH3+3Cl2═6NH4Cl+N2,3H2+N2$?_{催化剂}^{高温高压}$2NH3,能实现转化,故A不选;
B.SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,不能实现转化,故B选;
C.Al(OH)3+NaOH=NaAlO2+2H2O,NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 ,能实现转化,故C不选;
D.CH3COOCH2CH3+H2O$\frac{\underline{\;NaOH\;}}{△}$CH3CH2OH+CH3COOH,乙醇和乙酸发生酯化反应生成乙酸乙酯和水,化学反应为CH3CH2OH+CH3COOH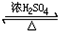 CH3COOCH2CH3+H2O,能实现转化,故D不选;
CH3COOCH2CH3+H2O,能实现转化,故D不选;
故选B.
点评 本题考查物质之间的化学反应,明确物质的性质是解本题关键,注意碳和二氧化硅反应生成硅和一氧化碳为制取粗硅的反应,为易错点,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
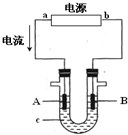 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作及现象 | ||
| A | 某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 溶液中一定含有CO32- |
| B | 将砂纸打磨过的铝箔置于酒精灯外焰上灼烧,熔化的铝以小液滴的形式滴落下来 | Al的熔点低,加热时Al熔化 |
| C | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中有Na+,无Κ+ |
| D | 向某溶液中先加几滴KSCN溶液,无明显现象,再滴加氯水,溶液变红 | 溶液中一定含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数由少到多的顺序:X=W<Y<Z | |
| B. | 原子半径由大到小的顺序:r(W)>r(X)>r(Y)>r(Z) | |
| C. | 元素非金属性由强到弱的顺序:X、Y、W | |
| D. | 元素的简单气态氢化物的稳定性由强到弱的顺序:Y、X、W |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
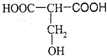 .
. +2H2O;
+2H2O;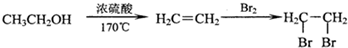
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
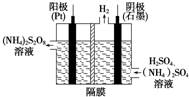 (1)过二硫酸铵法(如图所示)是目前最流行的制备H2O2的方法.即电解含H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8,再与热水反应即可得H2O2和(NH4)2SO4.
(1)过二硫酸铵法(如图所示)是目前最流行的制备H2O2的方法.即电解含H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8,再与热水反应即可得H2O2和(NH4)2SO4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:1 | B. | 1:4 | C. | 1:6 | D. | 6:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com