
| 简单实验方案 | 预测的实验现象 | 结论 |
| | | 假设____成立 |
| | 假设____成立 |

| 简单实验方案 | 预测的实验现象 | 结论 |
| 向褪色后的溶液中再加入过量NaOH溶液(1分) | 溶液又变红色 | ①(共1分) |
| 溶液颜色无变化(依然为无色) | ②(共1分) |


科目:高中化学 来源:不详 题型:单选题
| A.上述反应中氧化剂和还原剂的物质的量之比为5:6 |
| B.产生白色烟雾的原因是生成的P205白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾)形成气溶胶 |
| C.上述反应中消耗3 mol P时,转移电子的物质的量为15mol |
| D.因红磷和白磷互为同素异形体,所以上述火药中的红磷可以用白磷代替 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ZnCl2是氧化产物,又是还原产物 |
| B.ZnI2是氧化产物,又是还原产物 |
| C.ICl跟H2O的反应,ICl是氧化剂,H2O是还原剂 |
| D.ICl跟H2O的反应,是自身氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分解反应一定是氧化还原反应 |
| B.非金属单质在氧化还原反应中一定作氧化剂 |
| C.氧化剂具有氧化性,还原剂具有还原性 |
| D.氧化剂在氧化还原反应中被氧化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧气与臭氧的相互转化是非氧化还原反应 |
| B.稀硝酸是弱酸,浓硝酸是强酸 |
| C.相对分子质量相同,而结构不同的化合物互称为同分异构体 |
| D.共价化合物可能含离子键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过氧化钡的化学式为Ba2O2 |
B.O22-的电子式为: 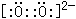 |
| C.反应Na2O2+2HCl==2NaCl+H2O2为氧化还原反应 |
| D.过氧化钡和过氧化钠都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 l2________ mL。
l2________ mL。 mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.
mol KBrO3在反应中得到1mol电子生成X,则X的化学式为______________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com