
|
已知:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O.现称取6.0 g含H2C2O4·2H2O、KHC2O4等的试样,加水溶解,配成250 mL溶液.量取两份此溶液各25.00 mL,分别置于两个锥形瓶中. ①第一份溶液中加入酚酞试液,滴加0.250 mol/L NaOH溶液至20.00 mL时,溶液由无色变为浅红色. ②第二份溶液中滴加0.100 mol/L的酸性高锰酸钾溶液至16.00 mL时,溶液颜色由无色变为紫红色.原试样中H2C2O4·2H2O的质量分数为 | |
| [ ] | |
A. |
2.1% |
B. |
12.3% |
C. |
1.2% |
D. |
21% |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.0 | 3.1 | 8.1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
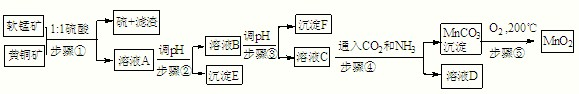
| Cu(OH)2 | Fe(OH)3 | Mn(OH)2 | Fe(OH)2 | |
| 开始沉淀pH | 4.2 | 1.5 | 7.3 | 6.4 |
| 完全沉淀pH | 6.7 | 3.2 | 9.8 | 9.0 |
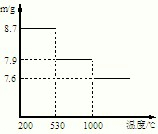
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 现象与结论 |
| 步骤1:向试管中加入少量固体产物,再加入足量 |
若溶液颜色明显改变,且有 |
| 步骤2:将步骤1中得到的浊液过滤,并用蒸馏水洗涤至洗涤液无色 | |
| 步骤3:取步骤2得到的少量固体与试管中,滴加 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com