
②CH2OH(CHOH)4CHO ③(C6H10O5)n(纤维素) ④HCOOC2H5 ⑤苯酚 ⑥HCHO等物质,其中(用数字序号填空):
(1)难溶于水的是_________,易溶于水的是_________,常温下微溶于水的是_________。
(2)能发生银镜反应的是________________。
(3)能发生酯化反应的是________________。
(4)能跟氢气发生加成反应的是_________,能在一定条件下跟水反应的是_________。
(5)能跟盐酸反应的是_________,能跟氢氧化钠溶液反应的是_________。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
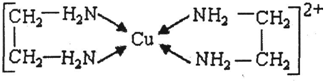
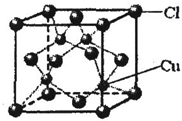
查看答案和解析>>
科目:高中化学 来源: 题型:
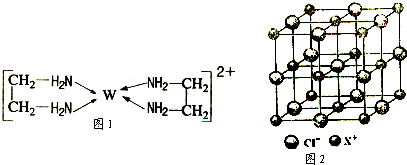
查看答案和解析>>
科目:高中化学 来源: 题型:
A、用甘氨酸(H2N-CH2-COOH)和丙氨酸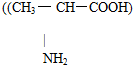 缩合最多可形成4种二肽 缩合最多可形成4种二肽 | B、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | C、苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构 | D、向鸡蛋清溶液中分别加入(NH4)2SO4和CuSO4溶液都能使鸡蛋清聚沉,其作用原理相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com