

分析 (1)从氯化钾溶液中得到氯化钾固体,为可溶性固体与液体的分离;除去自来水中的Cl-等杂质,利用沸点不同采取蒸馏法分离;
(2)碘不易溶于水,易溶于有机溶剂,可用萃取的方法分离;
(3)由图可知仪器的名称,冷水下进上出效果好,温度计测定馏分的温度;分液时,应打开活塞和塞子;
(4)粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,提纯过程中,先加水溶解,然后把杂质转化为沉淀或气体除去,除Ca2+用CO32-,除Mg2+、Fe3+用OH-,除SO42-用Ba2+.要注意除杂质的顺序,后加的试剂最好能把前面先加的过量试剂除掉.
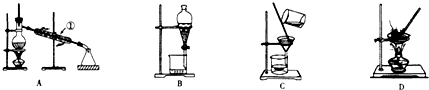
解答 解:(1)可以采用蒸发结晶的方法从氯化钾溶液中得到氯化钾固体,则选择D装置;除去自来水中的Cl-等杂质,可以采用蒸馏的方法,则选择A装置,故答案为:D;A;
(2)碘易溶于有机溶剂,可用萃取的方法分离,故答案为:B;萃取;
(3)装置A中①的名称是冷凝管,进水的方向是“下进上出”,否则水蒸气急剧冷却易产生爆炸,装置B在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是打开分液漏斗上端的玻璃塞,
故答案为:冷凝管;下;打开分液漏斗上端的玻璃塞;
(4)除去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42-时,先加水溶解,所以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓;加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,然后过滤,最后调节溶液的pH等于7后蒸发即可,所以其顺序是⑤③②①⑥④⑦或⑤②③①⑥④⑦,
故答案为:ad.
点评 本题考查物质的分离提纯及实验装置综合,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓H2SO4具有强氧化性是因为其中含+6价S,所有只要含最高价+6价S的化合物就具有强氧化性 | |
| B. | H2S中的S处于最低价,因此其不可能具有氧化性 | |
| C. | 浓H2SO4可把Na2SO3氧化 | |
| D. | 因为元素化合价变化以相邻价态之间转化最容易,因此发生氧化还原反应时,浓H2SO4对应的产物一般为SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
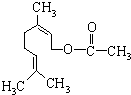 乙酸橙花酯是一种食用香料,结构如图.关于该物质的说法中正确的是( )
乙酸橙花酯是一种食用香料,结构如图.关于该物质的说法中正确的是( )| A. | ①②④ | B. | ③ | C. | ③⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+H2O+CO2↑ | B. | MgCO3+CO2+H2O═Mg(HCO3)2 | ||
| C. | MgCO3+H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑ | D. | CaCO3+H2O═Ca(OH)2+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KOH的摩尔质量是56 g | |
| B. | 一个碳原子的质量就是其相对原子质量 | |
| C. | 硫原子的质量就是硫的相对原子质量 | |
| D. | 氦气的摩尔质量以g•mol-1为单位时在数值上等于它的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.lmol•L-lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4-)>c(H2C2O4)>c(C2O42- ) | |
| B. | 0.lmol•L-1NaHS 溶液:C(OH-)+c(S2-)=c( H+)+c(H2S) | |
| C. | 0.lmol•L-1CH3COOH 溶液和 0.lmol•L-1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c( OH-) | |
| D. | 0.lmol•L-lNH4HSO4 溶液中滴加 0.lmol•L-1NaOH 溶液至中性:c(Na+ )>c(SO42- )>c(NH4+ )>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
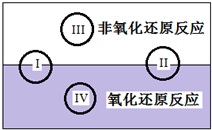 氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题:
氧化还原反应在生产、生活中具有广泛的用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ②③④ | C. | ③⑤ | D. | ④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com