



 +2NaHCO3→
+2NaHCO3→ +2CO2↑+2H2O.
+2CO2↑+2H2O. 、
、 .
. 分析 苹果酸的相对分子质量为134,C、H、O三种元素质量分数之和为100%,则苹果酸含有C、H、O三种元素,分子中N(C)=$\frac{134×35.8%}{12}$=4,N(H)=$\frac{134×4.48%}{1}$=6,N(O)=$\frac{134-12×4-6}{16}$=5,苹果酸的分子式为C4H6O5,1mol该酸与足量的NaHCO3反应放出44.8L CO2,说明分子中含有2个-COOH,与足量的Na反应放出33.6L H2,为1.5mol,说明分子中含有1个-OH,分子中氢原子处于5种不同的化学环境,则苹果酸结构简式为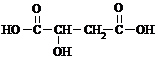
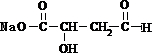 ,H酸化得到I为
,H酸化得到I为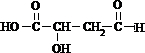 ,I发生氧化反应得到J为
,I发生氧化反应得到J为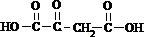 ,J与氢气发生加成反应得到苹果酸,据此解答.
,J与氢气发生加成反应得到苹果酸,据此解答.
解答 解:苹果酸的相对分子质量为134,C、H、O三种元素质量分数之和为100%,则苹果酸含有C、H、O三种元素,分子中N(C)=$\frac{134×35.8%}{12}$=4,N(H)=$\frac{134×4.48%}{1}$=6,N(O)=$\frac{134-12×4-6}{16}$=5,苹果酸的分子式为C4H6O5,1mol该酸与足量的NaHCO3反应放出44.8L CO2,说明分子中含有2个-COOH,与足量的Na反应放出33.6L H2,为1.5mol,说明分子中含有1个-OH,分子中氢原子处于5种不同的化学环境,则苹果酸结构简式为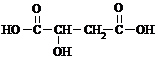
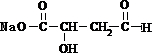 ,H酸化得到I为
,H酸化得到I为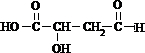 ,I发生氧化反应得到J为
,I发生氧化反应得到J为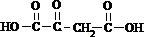 ,J与氢气发生加成反应得到苹果酸,
,J与氢气发生加成反应得到苹果酸,
(1)由上述分析可知,苹果酸的分子式为C4H6O5,
故答案为:C4H6O5;
(2)F为HO-CH2-COOH,含有的官能团名称是:羧基、羟基.
故答案为:羧基、羟基;
(3)G+B→H的反应类型是:加成反应,
故答案为:加成反应;
(4)在合成线路中,C→D这一步骤反应的目的是:在乙酸分子中引入Br原子,
故答案为:在乙酸分子中引入Br原子;
(5)D→E反应的化学方程式为:Br-CH2-COOH+2NaOH$→_{△}^{水}$HO-CH2-COONa+NaBr+H2O,
故答案为:Br-CH2-COOH+2NaOH$→_{△}^{水}$HO-CH2-COONa+NaBr+H2O;
(6)苹果酸与NaHCO3完全反应的化学方程式为: +2NaHCO3→
+2NaHCO3→ +2CO2↑+2H2O,
+2CO2↑+2H2O,
故答案为: +2NaHCO3→
+2NaHCO3→ +2CO2↑+2H2O;
+2CO2↑+2H2O;
(7)与苹果酸含有相同种类和数目的官能团的同分异构体的结构简式为:

故答案为:

点评 本题考查有机物的推断,注意计算确定苹果酸的分子式,结合含有的官能团及H原子种类判断苹果酸的结构简式,也可以利用乙烯发生的系列反应进行推断,是对有机化学的综合可知,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同.根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同.根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 发生酯化反应的产物.
发生酯化反应的产物. 、
、 、
、 (其中之一).
(其中之一).

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3 | B. | ${\;}_{1}^{1}$H与${\;}_{1}^{2}$H | ||
| C. | CH3CH3与CH3CH2 CH3 | D. | CH3CH2CH2CH3与 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④②① | C. | ④①②③ | D. | ③①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com