
| A. | H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O | |
| B. | Ba2++SO42-═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O | |
| C. | CO32-+2H+═CO2↑+H2O CaCO3+2HCl═CaCl2+CO2↑+H2O | |
| D. | Al(OH)3+OH-═AlO2-+2H2O Al(OH)3+NaOH═NaAlO2+2H2O |
分析 A.醋酸为弱酸不能完全电离;
B.水为弱电解质不能写成离子;
C.碳酸钙是难溶于水的固体,不能拆成离子;
D.氢氧化钠和偏铝酸钠都是易溶于水的强电解质.
解答 解:A.化学方程式中醋酸是弱酸不能完全电离,离子方程式中写分子式,CH3COOH+NaOH═CH3COONa+H2O的离子方程式为:CH3COOH+OH-═CH3COO-+H2O,故A错误;
B.Ba(OH)2+H2SO4═BaSO4↓+2H2O的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故B错误;
C.CaCO3+2HCl═CaCl2+CO2↑+H2O反应的离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O,故C错误;
D.Al(OH)3+NaOH═NaAlO2+2H2O的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质及离子反应方程式的意义,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 100mL 1mol/LAlCl3溶液 | B. | 200 mL 1mol/LMgCl2溶液 | ||
| C. | 100mL 0.5mol/LCaCl2溶液 | D. | 100 mL 2 mol/L KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 适当升高温度 | B. | 加入NH4Cl固体 | C. | 通入NH3 | D. | 加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
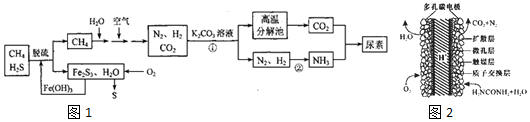
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 水电离的[H+]随着温度的升高而降低 | B. | 在35℃时,水电离的[H+]>[OH-] | ||
| C. | 水的电离程度:35℃>25℃ | D. | 水电离的[OH-]随温度升高而增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
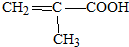 .
.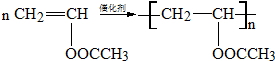 .
.
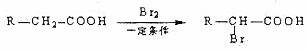 D可以发生如下转化关
D可以发生如下转化关 系:
系: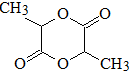 .并写出N发生消去反应的化学方程式CH3CH(OH)COOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.
.并写出N发生消去反应的化学方程式CH3CH(OH)COOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com