
【题目】(10分)常温下,现有A、B、C、D四种电解质分别完全溶于水,所得四种溶液中含H+、Ba2+、Al3+、Na+、HCO3-、Cl-、OH-、SO42-八种离子(不考虑水解)。为了检验这四种物质,进行如下实验:
①取少量A的溶液分别与另三种物质反应,依次观察到:白色沉淀和气体、气体、白色沉淀。
②经测定,A和D的溶液显碱性,B和C的溶液pH<7。B与D的溶液反应产生两种沉淀,当D的量增大时,其中一种沉淀不断溶解,最终还存在一种沉淀。
③C与D的溶液反应,无明显现象。经测定,该反应的产物总能量小于反应物总能量。
根据上述实验事实,请回答下列问题:
(1)C的名称是________,D的化学式_________。
(2)用离子方程式表示A的溶液显碱性的原因:_________________。
(3)A与B在溶液中反应的离子方程式为________________。
(4)等物质的量浓度、等体积的B和D的溶液混合,写出反应的离子方程式:_________________。
【答案】(10分)(各2分)(1)氯化氢;Ba(OH)2;
(2)HCO3-+H2O![]() H2CO3+OH-;
H2CO3+OH-;
(3)Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(4)3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓。
【解析】
试题分析:①取少量A的溶液分别与另三种物质反应,依次观察到:白色沉淀和气体、白色沉淀、气体,结合离子之间的反应现象来判断,铝离子和碳酸氢根离子反应既产生白色沉淀又产生气体;钡离子和碳酸氢根离子、氢氧根离子之间的反应产生白色沉淀;氢离子和碳酸氢根离子之间反应产生水以及二氧化碳,A是NaHCO3。②经测定,A和D的溶液显碱性,则含有氢氧根离子或是HCO3-,B和C的溶液pH<7,则含有氢离子或是铝离子等;B与D的溶液反应产生两种沉淀,当D的量增大时,其中一种沉淀不断溶解,最终还存在一种沉淀,则一定是硫酸铝和氢氧化钡之间的反应,所以D是Ba(OH)2 ,B是Al2(SO4)3,③C与D的溶液反应,无明显现象,该反应的产物总能量小于反应物总能量,该反应是放热反应,所以C是HCl,综上知道A是NaHCO3, B是Al2(SO4)3,C是HCl,D是Ba(OH)2。(1)据上述分析可知C是盐酸,化学式是HCl,D是Ba(OH)2;(2)A是NaHCO3,碳酸氢根离子水解导致溶液显示碱性,盐水解程度是微弱的,主要以盐电离产生的离子存在,水解反应方程式为:HCO3-+H2O![]() H2CO3 +OH-;(3)碳酸氢钠溶液和硫酸铝之间发生盐的双水解反应,产生氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑;(4)将等物质的量浓度、等体积的B和D的溶液混合,Al2(SO4)3过量,反应产生硫酸钡沉淀和氢氧化铝沉淀,反应的离子方程式是3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓。
H2CO3 +OH-;(3)碳酸氢钠溶液和硫酸铝之间发生盐的双水解反应,产生氢氧化铝沉淀和二氧化碳气体,反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑;(4)将等物质的量浓度、等体积的B和D的溶液混合,Al2(SO4)3过量,反应产生硫酸钡沉淀和氢氧化铝沉淀,反应的离子方程式是3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。I.在具支试管中加入碎瓷片和无水硫酸铝,用注射器吸取一定量石蜡油,重新连接好装置;点燃酒精灯,加热具支试管中的碎瓷片和无水硫酸铝的混合物约两分钟;将注射器中的石蜡油缓慢、逐次推入具支试管中,石蜡油与灼热的碎瓷片和无水硫酸铝接触,将所得气体依次通入酸性高锰酸钾溶液和溴水中,发现酸性高锰酸钾溶液和溴水均褪色.,将导气管迅速替换成燃烧尖嘴,点燃气体,火焰明亮,有黑烟。

(1)碎瓷片和无水硫酸铝的作用是___________。
(2)通过本实验说明____________________。
II.实验室可用氯气与金属铁反应制备无水三氯化铁,三氯化铁呈棕红色、易潮解,100![]() 左右时升华。某化学兴趣小组利用下列实验装置制备并收集无水三氯化铁。
左右时升华。某化学兴趣小组利用下列实验装置制备并收集无水三氯化铁。
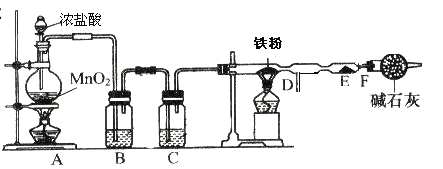
(3)A装置中发生反应的离子方程式为 ;
(4)实验时,先点燃A处的酒精灯,当D管处颜色变黄绿色时,再点燃D处的酒精灯,这样操作是为了 。
(5)B装置中应盛放的试剂名称为 ;
(6)F装置所起的作用是阻止空气中的水进入反应器,防止无水三氯化铁潮解和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g) ΔH = a kJ mol-1
2Fe(s)+3CO2(g) ΔH = a kJ mol-1
(1)已知: ①Fe2O3(s)+3C(石墨) = 2Fe(s)+3CO(g) ΔH1 = + 489.0 kJ mol-1
②C(石墨)+CO2(g) = 2CO(g) ΔH2 = + 172.5 kJ mol-1
则a = kJ mol-1。
(2)冶炼铁反应的平衡常数表达式K = ,温度升高后,K值 (填“增大”、“不变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe2O3 | CO | Fe | CO2 | |
甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
① 甲容器中CO的平衡转化率为 。
② 下列说法正确的是 (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在a-c装置中,能保护铁的是 (填字母)。
②若用d装置保护铁,X极的电极材料应是 (填名称)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高聚物的单体A(C11H12O2)可发生以下变化:

已知: C的烃基部分被取代生成的一氯代物D有两种;F的分子式为C7H8O,含有苯环,但与FeCl3溶液不显色。请回答:
(1)F分子中含有的官能团结构简式是 。
(2)由A生成B和F的反应类型为(选填序号) 。
①氧化反应 ②取代反应 ③水解反应 ④消去反应
(3)B的结构简式是 。
(4)分子式为C7H8O,含有苯环的同分异构体除F外还有 种。
(5)写出下列方程式
① 由A生成B和F: ;
② B → C: ;
③A在一定条件下生成高聚物: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫化合物的种类很多,现有SO2、Na2SO3、H2SO4、CuSO4四种常见的含硫化合物。回答下列问题:
(1)将SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是________.
A.S2- B.S C.SO32- D.SO42-
(2)亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现有试剂:溴水、H2S、稀硫酸。请选取合适的试剂证明Na2SO3具有还原性。所选试剂是_______,该反应的离子方程式为 .
(3)常温下,将铁棒置于浓硫酸中,无明显现象,有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面___________,则发生了钝化;若铁棒表面_____________,则未发生反应。
(4)用铜制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式
最佳途径是_______(填序号),理由是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图
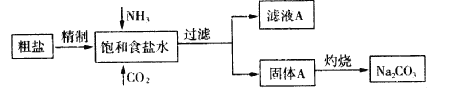
请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+,Mg2+,SO42-等。粗盐溶解之后,依次加入下列药品:
足量NaOH溶液、 、 除杂,然后过滤,向滤液中加入适量盐酸得到精制食盐水。
(2)向饱和食盐水中通氨气和二氧化碳反应的方程式为: 。
(3)可以区别A固体和Na2CO3固体的方法有 。
A.利用热稳定性不同,加热固体并将生成的气体通入澄清石灰水中,观察是否有浑浊
B.将相同浓度的盐酸逐滴滴入相同浓度的上述固体的溶液中,观察气体产生的速率
C.向相同浓度的两种固体的溶液中滴入酚酞试液,观察溶液颜色的深浅
D.取两种固体配成的溶液,分别加入BaCl2溶液,观察是否有固体生成
E.取两种固体配成的溶液,分别加入Ba(OH)2溶液,观察是否有固体生成
F.取两种固体配成的溶液,分别测量溶液的pH值并比较大小
(4)检验滤液A中含有的阳离子的方法为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜钱在历史上曾经是一种广泛流通的货币。从物理性质和化学性质的角度分析,铜常用于制造货币的说法正确的是( )
A.铜来源广泛,易于从自然界冶炼得到
B.铜的化学性质比较稳定,不易被腐蚀,铜的熔点比较低,容易冶炼铸造成型
C.铜的外观为紫红色,大方美观,易于被人们接受
D.铜的化学性质不稳定,在空气中易转化为铜绿,铜绿具有抗腐蚀能力,易于流通
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价,它们之间存在如下图的所示的转化关系。由此推断:
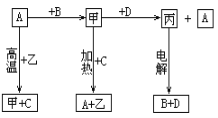
(1) 甲的化学式为________,丙的化学式为_________。
(2)写出甲和D反应的化学方程式_______________________。
(3)已知D能与烧碱溶液反应,写出D与烧碱溶液反应的离子方程式_______________。
(4)为检验化合物甲中元素的化合价,需要用到的药品有___________
A.稀硫酸
B.盐酸
C.硫氰化钾溶液
D.高锰酸钾溶液
(5)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:

化合物甲的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 甲烷(甲醛) | 银氨溶液 | 萃取 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com