
| A. | 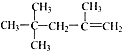 2,2,4-三甲基一4 一戊烯 2,2,4-三甲基一4 一戊烯 | |
| B. |  l,3,4一三甲苯 l,3,4一三甲苯 | |
| C. | CH3CH(CH3)CH(OH)CH3 2-甲基-3-丁醇 | |
| D. |  3,3,4-三甲基己烷 3,3,4-三甲基己烷 |
分析 A、烯烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
B、苯的同系物在命名时,从简单的侧链开始按顺时针或逆时针给主链上的碳原子进行编号,使侧链的位次和最小;
C、醇命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
D、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析.
解答 解:A、烯烃命名时,要选含官能团的最长的碳链为主链,故主链上有5个碳原子,为戊烯,从离官能团最近的一端给主链上的碳原子编号,故在1号和2号碳原子间有碳碳双键,在2号碳原子上有一个甲基,在4号碳原子上有2个甲基,并表示出官能团的位置,故名称为2,4,4-三甲基-1-戊烯,故A错误;
B、苯的同系物在命名时,从简单的侧链开始按顺时针或逆时针给主链上的碳原子进行编号,使侧链的位次和最小,故名称为1,2,4-三甲苯,故B错误;
C、醇命名时,要选含官能团的最长的碳链为主链,故在主链上有4个碳原子,为丁醇,从离官能团最近的一端给主链上的碳原子编号,故-OH在2号碳原子上,在3号碳原子上有一个甲基,故名称为3-甲基-2-丁醇,故C错误;
D、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,称为己烷,从离支链近的一端给主链上碳原子编号,当两端离支链一样近时,要从支链多的一端给主链上的碳原子编号,故名称为3,3,4-三甲基己烷,故D正确.
故选D.
点评 本题考查了有机物的命名,题目难度不大,该题注重了基础性知识的考查,侧重对学生基础知识的检验和训练.


科目:高中化学 来源: 题型:多选题
| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤中存在苯、二甲苯,工业上可由煤蒸馏获得 | |
| B. | 直馏汽油和裂化汽油中分别加入溴的四氯化碳溶液均能发生化学反应 | |
| C. | 石油的裂化、裂解和煤的干馏、气化都属于化学变化 | |
| D. | 石油裂解是生产乙烯的主要方法,乙烯和聚乙烯均能使溴水发生反应而褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl HCl H2O NaOH | B. | Cl2Na2S HCl CO2 | ||
| C. | HBr CCl4H2O CO2 | D. | Na2O2H2O2H2O O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )| A. | 所有碳原子不可能在同一平面上 | B. | 所有碳原子可能在同一条直线上 | ||
| C. | 碳原子同一平面上至少有9个 | D. | 所有原子可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不再发生变化 | |
| B. | 反应速率之比υ(N2):υ(H2):υ(NH3)=1:3:2 | |
| C. | 每生成3molH2的同时消耗2molNH3 | |
| D. | 每断裂1molN≡N键的同时断裂6molN-H键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com