
下列关于实验事故或药品的处理方法中,正确的是 ( )
A.少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗
B.大量氯气泄漏时,用肥皂水浸湿毛巾捂住嘴和鼻,并迅速离开现场
C.不慎洒出的酒精在桌上着火时,应立即用大量水扑灭
D.金属钠着火时,可立即用沾水的毛巾覆盖
科目:高中化学 来源: 题型:
用如图所示实验装置进行物质性质的探究实验。下列说法不合理的是 ( )
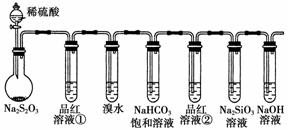
A.若品红溶液①褪色,则说明产物中含有SO2
B.若溴水褪色,则说明 SO2具有还原性
C.若烧瓶中产生黄色浑浊和无色气泡,则说明Na2S2O3只作氧化剂
D.若品红溶液②不褪色、Na2SiO3溶液中出现白色浑浊,则说明亚硫酸比碳酸的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是 ( )
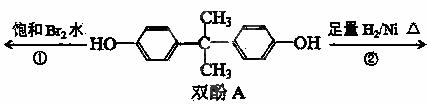
A.双酚A的相对分子质量为228
B.双酚A的核磁共振氢谱显示氢原子数之比为1:2:2:3
C.反应①中,1mol双酚A最多消耗2mol Br2
D.反应②的产物只有一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
元素性质呈周期性变化的决定因素是 ( )
A.元素原子半径大小呈周期性变化
B.元素的相对原子质量依次递增
C.元素原子核外电子排布呈周期性变化
D.元素的主要化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列相关实验不能达到预期目的的是( )
| 相关实验 | 预期目的 | |
| ① | 将SO2通入溴水,溴水褪色后加热观察能否恢复原色 | 验证SO2漂白的可逆性 |
| ② | 将氯气通入淀粉KⅠ溶液中 | 验证Cl的非金属性比Ⅰ强 |
| ③ | 在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率。 | 比较同周期金属元素的金属性强弱。 |
| ④ | 利用电解质溶液的导电性装置,检测AlCl3溶液的导电性 | 证明AlCl3是离子化合物 |
A.仅① B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
根据上述数据回答下列问题:
(1)下列物质本身具有的能量最低的是 。
A.H2 B.Cl2 C.Br2 D.I2
(2)相同条件下,X2 (X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是 。
(3)某烃在标准状况下的密度为3.215g/L,,现取3.6g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4g,碱石灰增重11g
则:①该烃的分子式为 ;
②该烃有多种同分异构体,其中与Cl2发生一氯取代的产物只有一种的烃的结构简式为:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
湖北荆门某化工厂违规快递有毒化学品,因泄漏导致9人中毒,1人死亡。涉事有毒化学品名为氟乙酸甲酯(C3H5O2F),其具有 结构的同分异构体还有(不考虑—O—F结构及立体异构)( )
结构的同分异构体还有(不考虑—O—F结构及立体异构)( )
A.4种 B.5种 C.6种 D.7种
查看答案和解析>>
科目:高中化学 来源: 题型:
苯甲酸乙酯(C9H10O2)别名为安息香酸乙酯,它是一种无色透明液体,不溶于水,稍有水果气味。用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为: +CH3CH2OH
+CH3CH2OH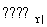
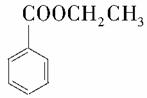 +H2O
+H2O
已知:
| 名称 | 相对分子质量 | 颜色、状态 | 沸点(℃) | 密度(g·cm-3) |
| 苯甲酸* | 122 | 无色、片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
*苯甲酸在100 ℃会迅速升华。
实验步骤如下:
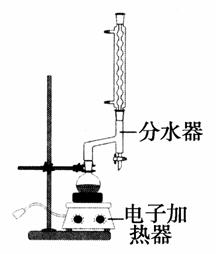
①在100 mL圆底烧瓶中加入12.20 g苯甲酸、25 mL 95%的乙醇(过量)、20 mL环己烷以及4 mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70 ℃加热回流2 h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213 ℃的馏分。
④检验合格,测得产品体积为12.86 mL。
回答下列问题:
(1)步骤①中加入沸石的作用是________________;如果加热一段时间后发现忘记加沸石,应该采用的正确操作是______________。
(2)步骤①中使用分水器不断分离除去水的目的是__________。
(3)步骤②中应控制馏分的温度在________。
A.65~70 ℃ B.78~80 ℃
C.85~90 ℃ D.215~220 ℃
(4)步骤③加入Na2CO3的作用是________________;采取分批加入Na2CO3而不是一次性加入的原因是________________;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是________________。
(5)关于步骤③中的分液操作叙述正确的是________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,将分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算本实验的产率为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置中发生反应2A2(g)+B2(g)2C(g) ΔH=-a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度时关闭K,向A、B容器中分别充入2 mol A2和1 mol B2,两容器分别在500 ℃时达平衡,A中C的浓度为w1 mol/L,放出热量b kJ,B中C的浓度为w2 mol/L,放出热量c kJ。请回答下列问题:
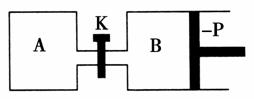
(1)此反应的平衡常数表达式为________________;若将温度升高到700 ℃,反应的平衡常数将________(填“增大”、“减小”或“不变”)。
(2)比较大小:w1________w2(填“>”、“=”或“<”),a、b、c由大到小的关系为________________。
(3)若打开K,一段时间后重新达平衡,容器B的体积将________
(填“增大”、“减小”或“不变”)。
(4)若让A、B体积相等且固定P,在B中改充入4 mol A2和2 mol B2,在500 ℃时达平衡后C的浓度为w3 mol/L,则w1、w3的关系为_________。
(5)能说明A中已达到平衡状态的是________________(填序号,有一个或多个选项符合题意)。
a.v(C)=2v(B2)
b.容器内气体压强保持不变
c.容器中气体的平均相对分子质量不随时间而变化
d.容器内的气体密度保持不变
(6)使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出C气体
b.适当升高温度
c.增大B2的浓度
d.选择高效的催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com