
·ÖĪö £Ø1£©¢Łøł¾ŻĶÖ»ÄÜŗĶÅØĮņĖį·“Ó¦ŗĶĻ”ĮņĖį²»·“Ó¦µÄŠŌÖŹÅŠ¶Ļ£»
¢Ś¼ÓČėĻõĖįÄĘĢį¹©ĻõĖįøłĄė×ÓŗĶČÜŅŗÖŠµÄĒāĄė×ÓŠĪ³ÉĻ”ĻõĖį£¬Ļ”ĻõĖįæÉŅŌŗĶ½šŹōĶÖ®¼ä·¢Éś·“Ó¦£»
£Ø2£©¹żĮæĶ·ŪÓėŅ»¶ØĮæÅØĻõĖį·“Ó¦£¬·“Ó¦æŖŹ¼ŹĒÉś³ÉNO2£¬·¢Éś£ŗCu+4HNO3=Cu£ØNO3£©2+2NO2”ü+2H2O£»Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ĻõĖįÅØ¶Č½µµĶ£¬Ļ”ĻõĖįÓėĶ·“Ӧɜ³ÉNO£¬·¢Éś£ŗ3Cu+8HNO3=3Cu£ØNO3£©2+2NO”ü+4H2O£»
£Ø3£©ŃĪĖį²»ÄÜÓė½šŹōĶ·“Ó¦£¬µ«æÉŅŌÓėŃõ»ÆĶ·“Ó¦£¬ĖłŅŌĖ«ŃõĖ®µÄ×÷ÓĆŹĒ½«½šŹōĶŃõ»ÆĪŖCuO£¬Č»ŗóŃõ»ÆĶČÜÓŚŃĪĖį£®
½ā“š ½ā£ŗ£Ø1£©¢ŚĶÖ»ÄÜŗĶÅØĮņĖį·“Ó¦£¬ŗĶĻ”ĮņĖį²»·“Ó¦£¬Cu+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+SO2”ü+H2O£¬ÅØĮņĖįµÄĪļÖŹµÄĮæĪŖ0.1L”Į18mol/L=1.8mol£¬Čē±»»¹ŌµÄĮņĖįŹĒ0.9mol£¬ŌņÉś³Én£ØSO2£©=0.9mol£¬V£ØSO2£©=0.9mol”Į22.4L/mol=20.16L£¬µ«Ėę×ÅĶŗĶÅØĮņĖįµÄ·“Ó¦µÄ½ųŠŠ£¬ĖįµÄÅضČŌ½Ą“Ō½Š”£¬²»ŌŁ²śÉś¶žŃõ»ÆĮņ£¬ŌņÉś³É¶žŃõ»ÆĮņµÄĢå»żŠ”ÓŚ20.16L£¬D·ūŗĻĢāŅā£¬
¹Ź“š°øĪŖ£ŗD£»
¢ŚČōŹ¹ÉĻŹö·“Ó¦¢ŁÖŠŹ£ÓąµÄĶʬ¼ĢŠųČܽā£¬æÉĻņĘäÖŠ¼ÓČėĻõĖįÄĘ£¬ĻõĖįøłĄė×ÓŌŚĖįŠŌ»·¾³ĻĀÄܹ»Ńõ»ÆĶÉś³ÉĻõĖįĶŗĶŅ»Ńõ»ÆµŖ”¢Ė®£¬Ąė×Ó·½³ĢŹ½£ŗ3Cu+8H++2NO3-=3Cu2++2NO”ü+4H2O£¬
¹Ź“š°øĪŖ£ŗ3Cu+8H++2NO3-=3Cu2++2NO”ü+4H2O£»
£Ø2£©¹żĮæµÄĶ·ŪÓėŅ»¶ØĮæÅØĻõĖį·“Ó¦£¬·“Ó¦æŖŹ¼ŹĒÉś³ÉNO2£¬·¢Éś£ŗCu+4HNO3=Cu£ØNO3£©2+2NO2”ü+2H2O£»Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ĻõĖįÅØ¶Č½µµĶ£¬Ļ”ĻõĖįÓėĶ·“Ӧɜ³ÉNO£¬·¢Éś£ŗ3Cu+8HNO3=3Cu£ØNO3£©2+2NO”ü+4H2O£»ĘųĢåµÄĪļÖŹµÄĮæĪŖ$\frac{1.12L}{22.4L/mol}$=0.05mol£¬µ±Éś³ÉĘųĢåČ«²æĪŖNO2Ź±£¬ĻūŗĵÄĻõĖįµÄĪļÖŹµÄĮæĪŖ0.05mol”Į2=0.10mol£¬µ±Éś³ÉĘųĢåČ«²æĪŖNOŹ±£¬ĻūŗĵÄĻõĖįµÄĪļÖŹµÄĮæĪŖ0.05mol”Į4=0.20mol£¬ĖłŅŌĻūŗĵÄĻõĖįµÄĪļÖŹµÄĮæ½éÓŚ0.10molŗĶ0.20molÖ®¼ä£¬Ö»ÓŠB·ūŗĻ£¬
¹Ź“š°øĪŖ£ŗNO2”¢NO£»B£»
£Ø3£©ŃĪĖį²»ÄÜÓė½šŹōĶ·“Ó¦£¬µ«æÉŅŌÓėŃõ»ÆĶ·“Ó¦£¬ĖłŅŌĖ«ŃõĖ®µÄ×÷ÓĆŹĒ½«½šŹōĶŃõ»ÆĪŖCuO£¬Č»ŗóŃõ»ÆĶČÜÓŚŃĪĖį£¬·“Ó¦µÄ·½³ĢŹ½ĪŖCu+H2O2+2HCl=CuCl2+2H2O£»
¹Ź“š°øĪŖ£ŗCu+H2O2+2HCl=CuCl2+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬²ąÖŲæ¼²éÅØĮņĖį”¢ĻõĖįµÄŠŌÖŹ£¬ŹģĻ¤¶žÕߊŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | N2H4£Øg£©+O2£Øg£©=N2£Øg£©+2H2O£Øg£©”÷H=-1 068 kJ/mol | |
| B£® | ėĀŹĒÓė°±ĄąĖʵÄČõ¼ī£¬ĖüŅ×ČÜÓŚĖ®£¬ĘäµēĄė·½³ĢŹ½£ŗN2H4+H2OØTN2H5++OH- | |
| C£® | ²¬×öµē¼«£¬ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗµÄėĀ--æÕĘųČ¼ĮĻµē³Ų£¬·ÅµēŹ±µÄøŗ¼«·“Ó¦Ź½£ŗN2H4-4e-+4OH-=N2+4H2O | |
| D£® | ²¬×öµē¼«£¬ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗµÄėĀ--æÕĘųČ¼ĮĻµē³Ų£¬¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬KOHČÜŅŗµÄpH½«Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
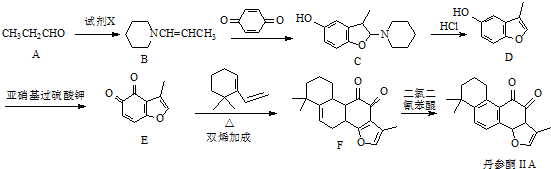
 £®
£® £®
£®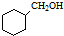 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮæÉČĪŃ”£©£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮæÉČĪŃ”£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·“Ó¦Īļ | äåĖ® | ĖįŠŌKMnO4ČÜŅŗ | ĒāĮņĖį£ØH2SČÜŅŗ£© | µĪÓŠ·ÓĢŖµÄNaOHČÜŅŗ | ŹÆČļŹŌŅŗ | Ę·ŗģČÜŅŗ |
| ·“Ó¦ĻÖĻó | ||||||
| SO2µÄŠŌÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļņ·ŠĖ®ÖŠµĪ¼Ó±„ŗĶĀČ»ÆĢśČÜŅŗ£ŗFe3++3H2O=Fe£ØOH£©3”ż+3H+ | |
| B£® | ĀČ»ÆŅųČÜÓŚÅØ°±Ė®£ŗAgCl+2NH3•H2O=[Ag£ØNH3£©2]Cl+2H2O | |
| C£® | ¹¤ŅµÉĻÖĘČ”ĘÆ°×·Ū£ŗCl2+2OH-=Cl-+ClO-+H2O | |
| D£® | NaNO2ČÜŅŗÖŠ¼ÓČėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£ŗ2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
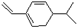 £¬øĆĢžŅŌĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1ÓėBr2¼Ó³ÉŹ±£¬ĖłµĆ²śĪļÓŠ£Ø””””£©
£¬øĆĢžŅŌĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1ÓėBr2¼Ó³ÉŹ±£¬ĖłµĆ²śĪļÓŠ£Ø””””£©| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4 L SO3ÖŠŗ¬ÓŠŃõŌ×ÓŹżÄæĪŖ3.0NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬12.0 gNaHSO4ÖŠŗ¬ÓŠĄė×Ó×ÜŹżĪŖ0.3NA | |
| C£® | ijĆܱÕČŻĘ÷Ź¢ÓŠ0.1 mol N2ŗĶ0.3 mol H2£¬ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦£¬×ŖŅʵē×ӵďżÄæĪŖ0.6NA | |
| D£® | ŌŚ1 L 0.1 mol•L-1Ģ¼ĖįÄĘČÜŅŗÖŠ£¬ŅõĄė×Ó×ÜŹż“óÓŚ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ņµ„ŃōĄė×ÓµÄŃõ»ÆŠŌ£ŗZ£¾X | |
| B£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗM£¾Y | |
| C£® | ¼ņµ„Ąė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ£ŗM£¾Y£¾Z | |
| D£® | ŌŚX2MÓėZ2MµÄČÜŅŗÖŠ£¬Ė®µÄµēĄė³Ģ¶Č£¬Ē°Õß“óÓŚŗóÕß |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com