
| A、K+.Ag+.Na+.Cl- |
| B、K+.Na+.NO3-.CO32- |
| C、Na+.H+.NO3-.SO42- |
| D、Fe3+.Na+.Cl-. SO42- |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-70.5 kJ?mol-1 |
| B、-44.1 kJ?mol-1 |
| C、70.5 kJ?mol-1 |
| D、44.1 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验时剩余的药品不能放回原瓶,所以实验时剩余的金属钠也不能放回原瓶 |
| B、某种气体通入品红溶液中,品红褪色,该气体一定是SO2 |
| C、焰色反应时观察到黄色火焰,说明样品中一定含钠元素可能含钾元素 |
| D、将铜片放入浓硫酸中,无明显现象,说明铜在冷浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
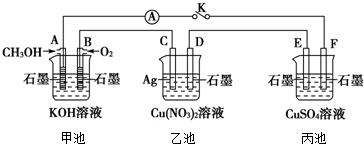
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| C、熵增加且吸热的反应一定是自发反应 |
| D、恒压条件下,反应的热效应等于焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该分散系放置一段时间可能很快出现分层现象 |
| B、有丁达尔效应 |
| C、不能透过滤纸 |
| D、所得分散系一定是浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol任何物质都含有约6.02×1023个原子 |
| B、常温常压下,4.4 g CO2气 体含有6.02×1022个CO2分子 |
| C、常温常压下28 g CO与22.4 L O2所含分子数相等 |
| D、标准状况下,33.6 L H2O含有9.03×1023个H2O分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com