
分析 (1)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性进行比较;
(2)具有强氧化性的物质能漂白,具有吸附性或能与有色物质反应生成无色物质的均能漂白;
(3)反应中I元素的化合价升高,Br元素的化合价降低,根据得失电子守恒和原子守恒配平方程式.
解答 解:(1)①KBrO3能把KI氧化成I2或KIO3,KBrO3本身被还原为Br2,则氧化性顺序是:KIO3<KBrO3,②Br2能把I-氧化为I2,氧化性是I2<Br2,
③KIO3能把I-氧化为I2,氧化性是:I2<KIO3,④KIO3能把Br-氧化为Br2,氧化性是:Br2<KIO3,综上氧化性顺序是:I2<Br2<KIO3<KBrO3,
故答案为:I2<Br2<KIO3<KBrO3;
(2)已知KBrO3具有强氧化性,具有强氧化性的物质能漂白;活性炭具有吸附性能漂白有色物质,二氧化硫能与有色物质反应生成无色物质,所以能漂白;
故答案为:KBrO3具有强氧化性;二氧化硫、活性炭;
(3)KI与KBrO3溶液反应生成I2、Br2,反应中I元素的化合价升高,Br元素的化合价降低,其反应的方程式为:10KI+2KBrO3+6H2SO4=K2SO4+5I2+Br2+6H2O;
故答案为:10KI+2KBrO3+6H2SO4=K2SO4+5I2+Br2+6H2O.
点评 本题考查了氧化还原反应,涉及氧化性强弱的判断以及电子守恒、元素守恒的应用等知识,注意知识的迁移和应用是关键,题目难度不大.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | X与Y形成原子个数比1:1的化合物只有2种 | |
| B. | Y、W的氧化物均为酸性氧化物 | |
| C. | 最高价氧化物对应水化物的酸性:Y<W | |
| D. | X与Z形成的化合物中,各原子均满足8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3溶液 | B. | NaCl溶液 | C. | 铜粉 | D. | 硫酸铜晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
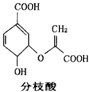
| A. | 可与乙醇、乙酸反应,且反应类型相同 | |
| B. | 1 mo1分枝酸最多可与3 mol NaOH发生中和反应 | |
| C. | 分枝酸的分子式为C10H8O6 | |
| D. | 分枝酸分子中含有2种官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com