
下列有关晶体的说法中一定正确的是
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
A.①③ B.只有⑤ C.②④⑤ D.③⑤
B
【解析】
试题解析:①原子晶体是原子之间通过共价键形成的晶体,同种元素原子之间形成非极性键,不同原子之间形成极性键,如二氧化硅是原子晶体,晶体中Si-O键是极性键,故错误;②稀有气体是单原子分子,分子之间通过分子间作用力形成分子晶体,故错误;③干冰晶体属于分子晶体,分子之间通过分子间作用力形成晶体,升华时分子间距增大,属于物理变化,破坏分子间作用力,没有破坏化学键,故错误;④金属元素和非金属元素形成的化合物可能是共价化合物,如氯化铝,故错误;⑤离子晶体由阴、阳离子通过离子键形成,金属晶体是金属离子与自由电子通过金属键形成,不存在离子键,故正确;故选B。
考点:化学键与晶体结构


科目:高中化学 来源:2015届四川省资阳市高三一诊理综化学试卷(解析版) 题型:选择题
下列实验的操作、现象、结论均正确的是
选项 | 操作 | 结论 |
A | 用洁净的铂金丝沾取硫酸盐在酒精灯上灼烧,焰色为黄色 | 该硫酸盐一定含Na 一定不含K |
B | 二氧化硫通入Ba(NO3)2溶液有白色沉淀生成,试管口出现浅红棕色气体 | 酸性条件下NO |
C | 在淀粉的水解液中加入新制Cu(OH)2悬浊液加热,无红色沉淀 | 淀粉没有发生水解 |
D | 某试样溶液中加入少量稀盐酸,有白色沉淀生成 | 试样中一定含有Ag |
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三(补习班)10月月考理综化学试卷(解析版) 题型:选择题
某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M离子,经测定Fe3+、SO42-、Al3+和M 离子的物质的量之比为2∶4∶1∶1,则M离子可能是下列中的
A、Na+ B、Cl- C、OH- D、S2-
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:选择题
下列有关实验操作、现象和解释或结论都正确的是
A.过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈红色,说明稀HNO3将Fe氧化为Fe3+
B.某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水,有白色沉淀出现,说明该钾盐是K2CO3
C.Al箔插入稀HNO3中,无现象,说明Al箔表面被HNO3氧化,形成致密的氧化膜
D.用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,浓氨水呈碱性
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:选择题
下列对一些实验事实的理论解释正确的是
| 实验事实 | 理论解释 |
A | SO2溶于水形成的溶液能导电 | SO2是电解质 |
B | 白磷为正四面体分子 | 白磷分子中P—P间的键角是109°28′ |
C | 1体积水可以溶解700体积氨气 | 氨是极性分子;可与水形成氢键;且与水反应 |
D | HF的沸点高于HCl | H—F的键长比H—Cl的键长短 |
查看答案和解析>>
科目:高中化学 来源:2015届吉林省长春外国语学校高三上学期期中理综化学试卷(解析版) 题型:填空题
(16分)氯气在298 K、100 kPa时,在1 L水中可溶解0.09 mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的化学方程式为________________________________________________;
(2)估算该反应的平衡常数________________________________(列式计算);
(3)在上述平衡体系中加入少量NaCl固体,平衡将向________移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将_______(填“增大”、“减小”或“不变”),平衡将向________移动。
(5)已知:H2CO3  HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3- + H+ Ka1(H2CO3) = 4.45×10-7
HCO3- CO32- + H+ Ka2(H2CO3) = 5.61×10-11
CO32- + H+ Ka2(H2CO3) = 5.61×10-11
HClO H+ + ClO- Ka(HClO) = 2.95×10-8
H+ + ClO- Ka(HClO) = 2.95×10-8
请依据以上碳酸和次氯酸的电离平衡常数,写出在下列条件下所发生反应的离子方程式:
将少量的氯气通入到过量的碳酸钠溶液中____________________________________;
(6)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。则下列选项中正确的是 。

A.MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
B.Mg与X2的反应是放热反应
C.化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
D.MgF2(s)+Br2(l)===MgBr2(s)+F2(g) ΔH=+600 kJ·mol- 1
依上图数据写出 MgBr2(s)与 Cl2(g)反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届吉林省长春外国语学校高三上学期期中理综化学试卷(解析版) 题型:选择题
已知HCN(aq)与NaOH(aq)反应生成1 mol正盐的ΔH=-12.1 kJ/mol;强酸、强碱的稀溶液反应的中和热ΔH=-57.3 kJ·mol-1。则HCN在水溶液中电离的ΔH等于
A.+69.4 kJ·mol-1 B.-69.4 kJ·mol-1
C.+45.2 kJ·mol-1 D.-45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三第三次月考化学试卷(解析版) 题型:选择题
已知:①2Zn(s)+O2(g)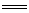 2ZnO(s)△H=-701.0kJ·mol-1
2ZnO(s)△H=-701.0kJ·mol-1
②2Hg(l)+O2(g)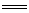 2HgO(s) △H=-181.6kJ·mol-1
2HgO(s) △H=-181.6kJ·mol-1
则反应Zn(s)+HgO(s)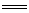 ZnO(s)+Hg(l)的△H为
ZnO(s)+Hg(l)的△H为
A.+519.4kJ·mol-1 B.+259.7kJ·mol-1
C.-259.7kJ·mol-1 D.-519.4kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015届吉林省吉林市高三第一次摸底考试化学试卷(解析版) 题型:选择题
某无色溶液中,已知含有H+、Mg2+、Al3+等阳离子,加入NaOH溶液的体积(v)和生成沉淀的质量(m)之间的关系如下图所示,其中正确的是
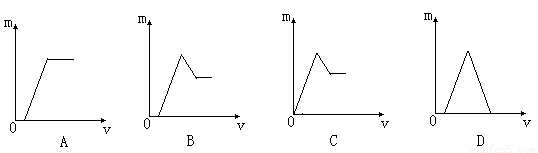
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com