
 H2O(g) + CO(g)��
H2O(g) + CO(g)��| A���ң��ף��� | B���ף������� | C���ң������� | D���ף��ң��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3(g) ��H����92.4kJ��mol��1����ش�
2NH3(g) ��H����92.4kJ��mol��1����ش� H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��
H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��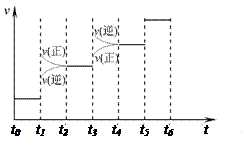
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 2SO3��g�������ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת���ʣ�������
2SO3��g�������ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת���ʣ�������| A������p%���� | B������p�� | C��С��p�� | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 g��+B��g��
g��+B��g�� nC��g����H=Q���ڲ�ͬ�����·�Ӧ�������C�İٷֺ�
nC��g����H=Q���ڲ�ͬ�����·�Ӧ�������C�İٷֺ� ���ͷ�Ӧ������ʱ��Ĺ�ϵ���ߡ������й�������һ����ȷ���ǣ���
���ͷ�Ӧ������ʱ��Ĺ�ϵ���ߡ������й�������һ����ȷ���ǣ���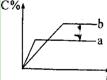
| A����ͼ����������жϣ���Ӧһ��������Ӧ����ʼ |
| B��ֻ�����¶ȣ���a��b���¶ȸߣ�Q��0 |
| C��ֻ����ѹǿ����a��b��ѹǿ��n��2 |
| D��������Ϊ���������ʾa�д�����b��ʾû�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2CO(g) ��
2CO(g) �� �����жϷ�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����
�����жϷ�Ӧ�Ѿ��ﵽ��ѧƽ��״̬����| A��v��CO2��= v��CO�� |
| B����������ѹǿ���� |
| C�������л��������ܶȲ��� |
| D��������CO������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 qZ��g����H;��Ӧ��Y�뷴Ӧʱ��t���¶�T��ѹǿp�Ĺ�ϵ������ͼ����ͨ���Դ����ߵķ������ж�������������ȷ����
qZ��g����H;��Ӧ��Y�뷴Ӧʱ��t���¶�T��ѹǿp�Ĺ�ϵ������ͼ����ͨ���Դ����ߵķ������ж�������������ȷ����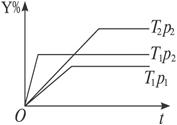
| A��T1��T2��p2��p1��m+n��q����H��0 |
| B��T1��T2��p2��p1��m+n��q����H��0 |
| C��T1��T2��p1��p2��m+n��q����H��0 |
| D��T1��T2��p1��p2��m+n��q����H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g) �˷�Ӧ�ﵽƽ��ı�־��
2Z(g) �˷�Ӧ�ﵽƽ��ı�־��| A��������ѹǿ����ʱ��仯 |
| B�������ڸ����ʵ�Ũ�Ȳ���ʱ��仯 |
| C��������X��Y��Z��Ũ��֮��Ϊl : 2 : 2 |
| D����λʱ������0.1 mol Xͬʱ����0.2 mol Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ag���̣���Fe3��������Ӧ���ȣ�
Ag���̣���Fe3��������Ӧ���ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO2�CQ��Q>0������N2O4��NO2Ũ�ȱ仯��ͼ��ʾ��
2NO2�CQ��Q>0������N2O4��NO2Ũ�ȱ仯��ͼ��ʾ��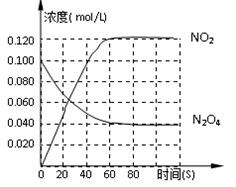
|
 0s��ƽ�����淴Ӧ�����ƶ������ܵ�ԭ���ǣ� ��
0s��ƽ�����淴Ӧ�����ƶ������ܵ�ԭ���ǣ� ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com