
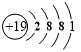 .
.分析 (1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,原子核外电子排布为1s22s22p3;
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,则乙为Cl元素、丙为K元素;
(3)丁元素的正三价离子的3d能级为半充满,原子核外电子排布式为1s22s22p63s23p63d64s2;
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子排布为1s22s22p63s23p63d104s1.
解答 解:(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,原子核外电子排布为1s22s22p3,为N元素,故答案为:N;
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,则乙为Cl元素、丙为K元素,K原子结构示意图为: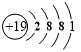 ,故答案为:Cl;
,故答案为:Cl;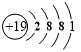 ;
;
(3)丁元素的正三价离子的3d能级为半充满,原子核外电子排布式为1s22s22p63s23p63d64s2,为Fe元素,故答案为:Fe;1s22s22p63s23p63d64s2;
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子排布为1s22s22p63s23p63d104s1,元素在周期表中位置为:第四周期第ⅠB族,故答案为:第四周期第ⅠB族;3d104s1.
点评 本题考查结构性质位置关系应用,侧重对核外电子排布规律的考查,难度不大,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①⑤⑥ | C. | ②③④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和Cu2O的物质的量之比为2:1 | |
| B. | 产生的NO在标准状况下的体积为4.48L | |
| C. | 硝酸的物质的量浓度为2.6mol•L-1 | |
| D. | Cu和Cu2O与硝酸反应后剩余HNO3为0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
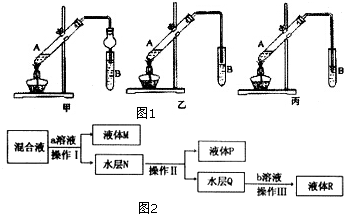
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH的电离程度变大 | B. | c(CH3COO-)增大 | ||
| C. | CH3COOH的Ka不变 | D. | 溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠与水反应比金属钠与甲醇反应更剧烈 | |
| B. | 结合H+的能力CH3O-<OH- | |
| C. | 所得到溶液中K=c(CH3O-)×c(CH3OH2+) | |
| D. | 所得到溶液中c(Na+)+c(CH3OH2+)═c(CH3O-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②⑤⑥ | C. | ③④ | D. | ①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 等物质的量浓度溶液的pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | a mol•L-1HCN溶液与b mol•L-1NaOH溶液等体积混合后,所得溶液中:c(Na+)>c(CN-),则a一定小于b | |
| C. | 往冰醋酸中逐滴加水,溶液的导电性逐渐增大 | |
| D. | 将0.2 mol•L-1 KHCO3溶液与0.1 mol•L-1 KOH溶液等体积混合:c(K+)+c(H+)=c(OH-)+c(HCO${\;}_{3}^{-}$)+2c(CO${\;}_{3}^{2-}$) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com