
下列物质中含有共价键的离子化合物是()
A. Ba(OH)2 B. H2O C. HCl D. CaCl2
考点: 离子化合物的结构特征与性质.
分析: 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,据此分析解答.
解答: 解:A.Ba(OH)2中钡离子和氢氧根离子之间存在离子键、O﹣H之间存在共价键,为离子化合物,故A正确;
B.水分子中O﹣H之间只存在共价键,为共价化合物,故B错误;
C.HCl分子中H﹣Cl之间只存在共价键,为共价化合物,故C错误;
D.氯化钙中钙离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选A.
点评: 本题考查化学键和化合物的关系,熟悉常见物质构成微粒及微粒之间作用力,注意这几个概念间的区别和联系,题目难度不大.


科目:高中化学 来源: 题型:
1体积某气态烃只能与1体积氯气发生加成反应生成氯代烷.1mol此氯代烷可与6mol氯气发生完全的取代反应,则该烃的结构简式为( )
|
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3CH3 | D. | CH3CH2CH=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据如图所示图象,写出反应的热化学方程式并回答下列问题:
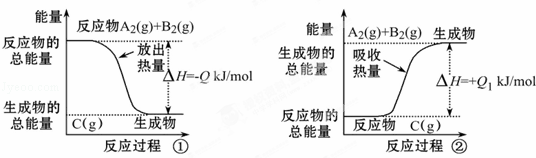
(1)反应过程①的热化学方程式为 :
(2)反应过程②的热化学方程式为:
(3)Q与Q1的关系:Q=Q1(填“<”、“>”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关C、N、S等非金属元素化合物的说法正确的是( )
A.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
B.SO2具有漂白性可以使酸性高锰酸钾溶液褪色
C.实验室可用NaOH溶液处理NO2和SO2废气
D.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
从固体混合物A出发可以发生如下框图所示的一系列变化。
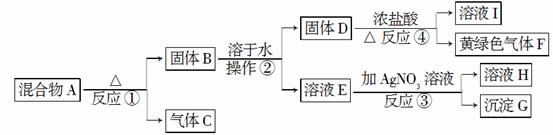
G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察)。回答下列问题:
(1)在实验室中收集气体C,可选择如图装置中的________。
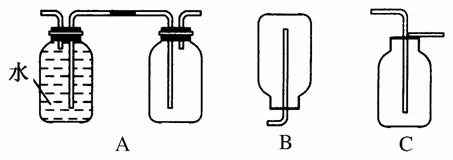
(2)操作②的名称是________。在操作②中所使用的玻璃仪器的名称是________。在得到固体D时必须进行洗涤、干燥等操作,洗涤固体D的目的是________________________________________。
(3)写出反应①的化学方程式、反应④的离子方程式:
反应①:_____________________________________________,
反应④:___________________________________________。
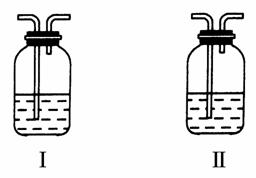
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它依次通过如图中的Ⅰ、Ⅱ装置,其中瓶Ⅰ中盛放的是________,瓶Ⅱ中盛放的是________。
(5)实验中必须吸收多余的气体F,以免污染空气。下图是实验室用NaOH溶液吸收气体F的装置,为防止产生倒吸现象,合理的装置是________。
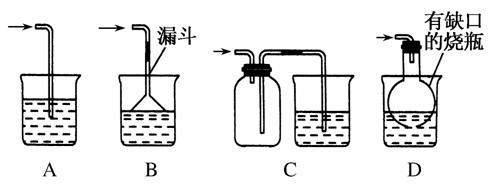
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L的密闭容器中进行反应:3H2+N2 2NH3,经过一段时间后,NH3的物质的量增加0.8mol,在这段时间内用N2表示的平均反应速率为0.01mol•l﹣1•s﹣1.则这段时间为()
2NH3,经过一段时间后,NH3的物质的量增加0.8mol,在这段时间内用N2表示的平均反应速率为0.01mol•l﹣1•s﹣1.则这段时间为()
A. 10s B. 20s C. 30s D. 40s
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是()
A. 氯化钙的电子式: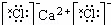
B. 168O2﹣离子的结构示意图: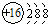
C. H2CO3的电离方程式:H2CO3⇌2H++CO32﹣
D. 葡萄糖的结构简式:C6H12O6
查看答案和解析>>
科目:高中化学 来源: 题型:
已知,将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3 ,且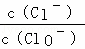 的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
的值与温度高低有关,当n(KOH)=a mol时,下列有关说法错误的是()
A. 若某温度下,反应后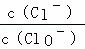 =11,则溶液中
=11,则溶液中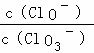 =
=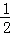
B. 参加反应的氯气的物质的量小于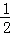 a mol
a mol
C. 改变温度,反应中转移电子的物质的量ne的范围: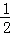 a mol≤ne≤
a mol≤ne≤ a mol
a mol
D. 改变温度,产物中KC1O3的最大理论产量为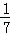 a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应方程式为:
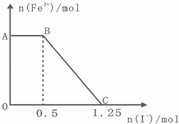 2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液(假设I﹣与KMnO4反应的氧化产物为I2),混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液(假设I﹣与KMnO4反应的氧化产物为I2),混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
A.图中AB段主要是高锰酸钾和碘化钾溶液反应
B.图中BC段发生的反应为2Fe3++2I﹣═2Fe2++I2通电
C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol
D.以Pt为电极材料电解C点的溶液,总反应式为2H2O 2H2↑+O2↑,则当外电路电子流通4mol时两极产生的气体总体积一定是67.2L
2H2↑+O2↑,则当外电路电子流通4mol时两极产生的气体总体积一定是67.2L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com