
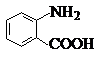 中官能团的名称氨基、羧基.
中官能团的名称氨基、羧基.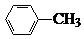 +Cl2$\stackrel{光}{→}$
+Cl2$\stackrel{光}{→}$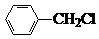 +HCl.
+HCl.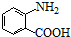 多一个碳的同系物,则满足下列条件的D的同分异构体共有19种,写出一种满足条件且含4种不同氢原子的同分异构体的结构简式
多一个碳的同系物,则满足下列条件的D的同分异构体共有19种,写出一种满足条件且含4种不同氢原子的同分异构体的结构简式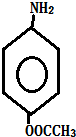 等.
等. .
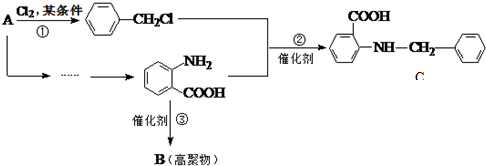
. 分析 (1)根据有机物 的结构简式可知,分子中官能团为氨基和羧基;
的结构简式可知,分子中官能团为氨基和羧基;
(2)由反应①是甲苯分子中甲基上氢原子被氯原子取代;
(3)根据反应②前后有机物结构简式的变化可知该反应的类型;
(4)D是比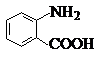

(5)由 生成
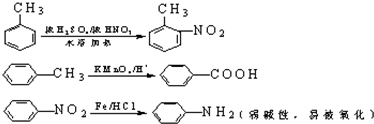
生成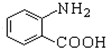 ,要将甲基氧化成羧基,将硝基还成氨基,由于氨基易被氧化,而羧基不易被还原,所以要先氧化甲基再还原硝基.
,要将甲基氧化成羧基,将硝基还成氨基,由于氨基易被氧化,而羧基不易被还原,所以要先氧化甲基再还原硝基.
解答 解:(1)根据有机物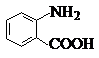
故答案为:氨基、羧基;
(2)反应①是甲苯分子中甲基上氢原子被氯原子取代,反应的化学方程式为: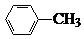
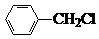
故答案为: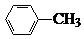
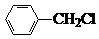
(3)根据反应前后有机物结构简式的变化可知,该反应是氨基中的氢原子被 取代,因此该反应是取代反应,
取代,因此该反应是取代反应,
故答案为:取代;
(4)D是比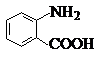

 ,氨基对位的取代基也可以是-COOCH3,
,氨基对位的取代基也可以是-COOCH3,
故答案为:19; 等;
等;
(5)由于氨基易被氧化,所以首先引入硝基后先氧化甲基,最后再还原硝基为氨基,所以正确的合成路线为: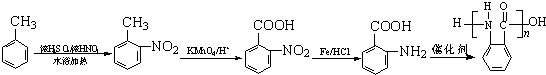 ,
,
故答案为: .
.
点评 本题考查有机合成,题目难度中等,解题时注意对给予信息的利用,(5)中注意先氧化甲基后再还原硝基,较好地考查学生分析推理能力、知识迁移运用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | 切开金属钠,钠表面的银白色会逐渐变暗 | Na在空气中会生成Na2O2 |
| B | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| C | SO2通入酸性KMnO4溶液,溶液褪色 | SO2具有漂白性 |
| D | 将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的$\frac{2}{3}$处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 | 从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
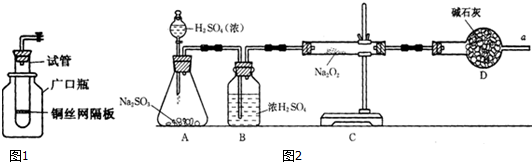
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
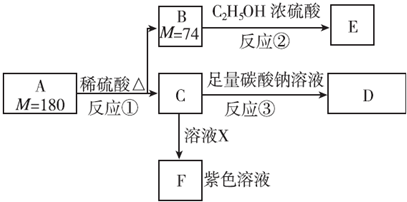
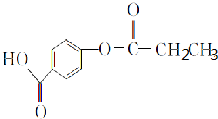 ,1 mol A与足量NaOH溶液反应的化学方程式为
,1 mol A与足量NaOH溶液反应的化学方程式为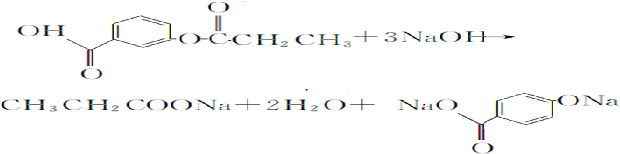 .
.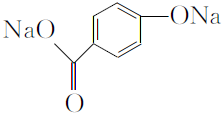 .
.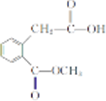 和
和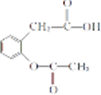 ,.
,.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
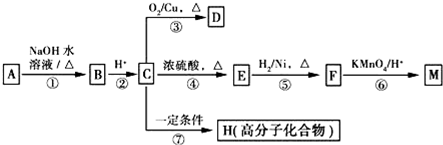
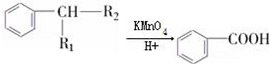 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)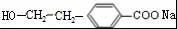 .
.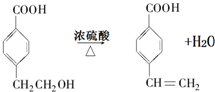 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
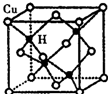 科学研究表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)
科学研究表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.0gCuO和Cu2S的混合物含铜原子个数为0.2NA | |
| B. | 标准状况下,11.2 L乙醇蒸气含共价键数目为4NA | |
| C. | 1mol K与O2完全反应生成K2O、K2O2、KO3的混合物,转移电子数为NA | |
| D. | 1L 0.2 mol•L-1 NH4ClO4溶液中含NH4+数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaOH溶液:c(CH3COONa)>c(C6H5ONa )>c(Na2CO3)>c(NaOH ) | |
| B. | 在常温下,10 mL 0.02 mol•L-1HCl溶液与10 mL 0.02 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10 | |
| C. | 将pH=3的一元弱酸HA和pH=11的NaOH溶液充分混合后一定有:c(OH-)<c(H+)<c(Na+)<c(A-) | |
| D. | 将0.2 mol•L-1的盐酸与0.1 mol•L-1的NaAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(Na+)<c(Cl-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com