
 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:分析 (1)根据化学平衡常数的概:平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,注意固体度为常数,不写入;
(2)对于放热反应,反应热△H<0;对于放热反应,温度升高,平衡逆向移动,K减小;根据速率之比等于化学计量数之比计算;
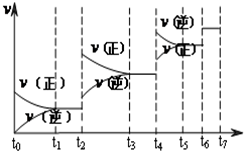
(3)若不改变H2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为压缩体积增大压强,由(2)已知反应为放热反应,升高温度速率加快,反应逆向移动也可;
(4)t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂,t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;
(5)已知:①2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol-1;
②H2O(g)=H2O(l)△H=-44kJ•mol-1,根据盖斯定律,结合燃烧热的概念可得答案.
解答 解:(1)可逆反应3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)的平衡常数K=$\frac{{c}^{6}(CO)}{{c}^{2}({N}_{2})}$;
故答案为:K=$\frac{{c}^{6}(CO)}{{c}^{2}({N}_{2})}$
(2)对于放热反应,反应热△H<0;对于放热反应,温度升高,平衡逆向移动,K减小;已知CO生成速率为v(CO)=18mol•L-1•min-1,根据速率之比等于化学计量数之比,则N2消耗速率为v(N2)=$\frac{1}{3}$×18mol•L-1•min-1=6mol•L-1•min-1;
故答案为:<;减小; 6mol•L-1•min-1
(3)若不改变H2、CO的量,由图可知,t4时瞬间正、逆反应都增大,平衡向逆反应移动,改变条件为压缩体积增大压强,由(2)已知反应为放热反应,升高温度速率加快,反应逆向移动也可;
故答案为:增大压强或升高温度
(4)t6时瞬间正、逆反应都增大,平衡不移动,故应是加入催化剂,t2时改变改变条件,平衡向正反应移动,在t3时重新到达平衡,t4时改变条件,平衡向逆反应移动,t5时由达平衡,故t3~t4平衡状态CO的含量最高;
故答案为:t3~t4
(5)已知:①2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol-1;
②H2O(g)=H2O(l)△H=-44kJ•mol-1,
根据燃烧热的热化学方程式的概念:1mol可燃物充分燃烧生成稳定氧化物的热化学方程式,由盖斯定律:
$①×\frac{1}{2}$+②可得:H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=-285.8•mol-1;
故答案为:H2(g)+$\frac{1}{2}$ O2(g)═H2O(l);△H=-285.8 kJ•mol-1
点评 考查化学平衡常数与影响因素、影响平衡移动的因素、化学反应速率计算、盖斯定律等,比较基础,注意方程式中物质的状态和燃烧热的概念,注意基础知识的掌握.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥⑦ | B. | ②⑤⑥⑦ | C. | ①③④⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molOH-所含质子数为10NA | |
| B. | 常温常压下,28克CO和N2的混合气体所含原子数为2NA | |
| C. | 4g氢气中含有的原子数为2NA | |
| D. | 标准状况下,11.2L酒精含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇可作为燃料电池的原料.通过下列反应可以制备甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ•mol-1在一容积可变的密闭容器中充入10mol CO 和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20L.
甲醇可作为燃料电池的原料.通过下列反应可以制备甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ•mol-1在一容积可变的密闭容器中充入10mol CO 和20mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
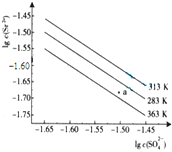
| A. | 温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 | |
| B. | 三个不同温度中,313K时Ksp(SrSO4)最小 | |
| C. | 283K时,图中a点对应的溶液是不饱和溶液 | |
| D. | 283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 灼烧的铁丝在氯气中燃烧,集气瓶内充满棕黄色烟雾 | |
| B. | 氢气在氯气中燃烧,集气瓶口有白雾 | |
| C. | 向盛水的烧杯中先加入过氧化钠,再滴加酚酞,最终溶液呈红色 | |
| D. | 将Cl2通入紫色石蕊溶液中,溶液变红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com