
| A. | ①②③④⑤⑥ | B. | ①④⑤ | C. | ②③④ | D. | ③④ |
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:解答题
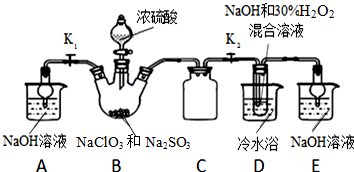
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳、甲烷、水汽等都是重要的温室气体 | |
| B. | 化学反应一定伴随能量变化,有能量变化也一定伴随化学反应 | |
| C. | 反应物所具有的总能量比生成物所具有的总能量高的反应是吸热反应 | |
| D. | Ba(OH)2•8H2O与NH4Cl的反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
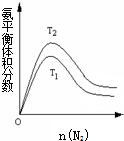 合成氨工业对国民经济和社会发展具有重要的意义.其原理为:
合成氨工业对国民经济和社会发展具有重要的意义.其原理为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁铝合金质量轻、强度大,可用作高铁车厢材料 | |
| B. | 用纸制品、聚乳酸等物质来替代聚乙烯产品,以减少白色污染 | |
| C. | 明矾可用于水的消毒、杀菌 | |
| D. | 大量燃烧化石燃料,是造成雾霾天气的一种原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| B. | 甲醛、氯乙烯和乙二醇均可作为合成聚合物的单体 | |
| C. | ABS树脂、光导纤维及碳纤维都是有机高分子材料 | |
| D. | 酸性条件下,C2H5CO18OC2H5的水解产物是C2H5CO18OH和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
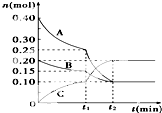 向10L的密闭容器中0.40mol A气体和0.20mol B气体,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:
向10L的密闭容器中0.40mol A气体和0.20mol B气体,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com