
”¾ĢāÄæ”æ»ÆѧŠĖȤŠ”×é¶ŌÄ³Ę·ÅĘŃĄøąÖŠÄ¦²Į¼Į³É·Ö¼°Ęäŗ¬Įæ½ųŠŠŅŌĻĀĢ½¾æ£ŗ²éµĆ׏ĮĻ£ŗøĆŃĄøąÄ¦²Į¼ĮÓÉĢ¼ĖįøĘ”¢ĒāŃõ»ÆĀĮ×é³É£»ŃĄøąÖŠĘäĖü³É·ÖÓöµ½ŃĪĖįŹ±ĪŽĘųĢåÉś³É£®
£Ø1£©¢ń£®Ä¦²Į¼ĮÖŠĒāŃõ»ÆĀĮµÄ¶ØŠŌ¼ģŃéČ”ŹŹĮæŃĄøąŃłĘ·£¬¼ÓĖ®³É·Ö½Į°č”¢¹żĀĖ£®
¢ŁĶłĀĖŌüÖŠ¼ÓČė¹żĮæNaOHČÜŅŗ£¬¹żĀĖ£®ĒāŃõ»ÆĀĮÓėNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ £®
¢ŚĶł¢ŁĖłµĆĀĖŅŗÖŠĻČĶØČė¹żĮ涞Ńõ»ÆĢ¼£¬ŌŁ¼ÓČė¹żĮæĻ”ŃĪĖį£®¹Ū²ģµ½µÄĻÖĻóŹĒ £®
£Ø2£©¢ņ£®ŃĄøąŃłĘ·ÖŠĢ¼ĖįøʵĶØĮæ²ā¶ØĄūÓĆČēĶ¼ĖłŹ¾×°ÖĆ£ØĶ¼ÖŠ¼Š³ÖŅĒĘ÷ĀŌČ„£©½ųŠŠŹµŃ飬³ä·Ö·“Ó¦ŗ󣬲ā¶ØCÖŠÉś³ÉµÄBaCO3³ĮµķÖŹĮ棬ŅŌČ·¶ØĢ¼ĖįøʵÄÖŹĮæ·ÖŹż£®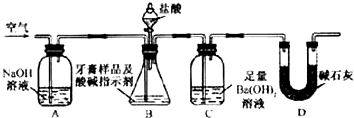
ŅĄ¾ŻŹµŃé¹ż³Ģ»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁŹµŃé¹ż³ĢÖŠŠč³ÖŠų»ŗ»ŗĶØČėæÕĘų£®Ęä×÷ÓĆ³żĮĖæɽĮ°čB”¢CÖŠµÄ·“Ó¦ĪļĶā£¬»¹ÓŠ£ŗ £®
¢ŚCÖŠ·“Ӧɜ³ÉBaCO3µÄ»Æѧ·½³ĢŹ½ŹĒ £®
¢ŪĻĀĮŠø÷Ļī“ėŹ©ÖŠ£¬²»ÄÜĢįøß²ā¶Ø×¼Č·¶ČµÄŹĒ£ØĢī±źŗÅ£©£®
a£®ŌŚ¼ÓČėŃĪĖįÖ®Ē°£¬Ó¦Åž»×°ÖĆÄŚµÄCO2ĘųĢå
b£®µĪ¼ÓŃĪĖį²»ŅĖ¹żæģ
c£®ŌŚA©BÖ®¼äŌöĢķŹ¢ÓŠÅØĮņĖįµÄĻ“Ęų×°ÖĆ
d£®ŌŚB©CÖ®¼äŌöĢķŹ¢ÓŠ±„ŗĶĢ¼ĖįĒāÄĘČÜŅŗµÄĻ“Ęų×°ÖĆ
¢ÜŹµŃéÖŠ×¼Č·³ĘČ”8.00gѳʷȿ·Ż£¬½ųŠŠČż“Ī²ā¶Ø£¬²āµĆBaCO3Ę½¾łÖŹĮæĪŖ3.94g£®Ōņѳʷ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżĪŖ £®
¢ŻÓŠČĖČĻĪŖ²»±Ų²ā¶ØCÖŠÉś³ÉµÄBaCO3ÖŹĮ棬ֻŅŖ²ā¶Ø×°ÖĆCŌŚĪüŹÕCO2Ē°ŗóµÄÖŹĮæ²ī£¬Ņ»ŃłæÉŅŌČ·¶ØĢ¼ĖįøʵÄÖŹĮæ·ÖŹż£®ŹµŃéÖ¤Ć÷°““Ė·½·Ø²ā¶ØµÄ½į¹ūĆ÷ĻŌĘ«øߣ¬ŌŅņŹĒ £®
”¾“š°ø”æ
£Ø1£©Al£ØOH£©3+OH©ØTAlO2©+2H2O£»ĶØČėCO2ĘųĢåÓŠ°×É«³ĮµķÉś³É£»¼ÓČėŃĪĖįÓŠĘųĢå²śÉś£¬³ĮµķČܽā
£Ø2£©°ŃÉś³ÉµÄCO2ĘųĢåČ«²æÅÅČėCÖŠ£¬Ź¹Ö®ĶźČ«±»Ba£ØOH£©2ČÜŅŗĪüŹÕ£»CO2+Ba£ØOH£©2ØTBaCO3”ż+H2O£»cd£»25%£»BÖŠµÄĖ®ÕōĘų”¢ĀČ»ÆĒāĘųĢåµČ½ųČė×°ÖĆCÖŠ
”¾½āĪö”æ½ā£ŗ£Ø1£©¢Ł¢ń£®ĒāŃõ»ÆĀĮÓėNaOHČÜŅŗ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘÓėĖ®£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+OH©ØTAlO2©+2H2O£¬ĖłŅŌ“š°øŹĒ£ŗAl£ØOH£©3+OH©ØTAlO2©+2H2O£»¢ŚĶł¢ŁĖłµĆĀĖŅŗÖŠĻČĶØČė¹żĮ涞Ńõ»ÆĢ¼£¬·¢Éś·“Ó¦AlO2©+CO2+2H2O=Al£ØOH£©3”ż+HCO3© £¬ ŌŁ¼ÓČė¹żĮæĻ”ŃĪĖį£¬Al£ØOH£©3+3HCl=AlCl3+3H2O£¬HCO3©+H+=CO2”ü+H2O£¬·“Ó¦ĻÖĻóŹĒĶØČėCO2ĘųĢåÓŠ°×É«³ĮµķÉś³É£»¼ÓČėŃĪĖįÓŠĘųĢå²śÉś£¬³ĮµķČܽā£¬ĖłŅŌ“š°øŹĒ£ŗĶØČėCO2ĘųĢåÓŠ°×É«³ĮµķÉś³É£»¼ÓČėŃĪĖįÓŠĘųĢå²śÉś£¬³ĮµķČܽā£»£Ø2£©¢ņ£®¢Ł×°ÖĆÖŠ²ŠĮō²æ·Ö¶žŃõ»ÆĢ¼£¬²»Äܱ»ĶźČ«ĪüŹÕ£¬µ¼ÖĀ²ā¶ØµÄĢ¼Ėį±µµÄÖŹĮæĘ«Š”£¬³ÖŠų»ŗ»ŗĶØČėæÕĘųµÄ×÷ÓĆĪŖ£ŗ°ŃÉś³ÉµÄCO2ĘųĢåČ«²æÅÅČėCÖŠ£¬Ź¹Ö®ĶźČ«±»Ba£ØOH£©2ČÜŅŗĪüŹÕ£¬ĖłŅŌ“š°øŹĒ£ŗ°ŃÉś³ÉµÄCO2ĘųĢåČ«²æÅÅČėCÖŠ£¬Ź¹Ö®ĶźČ«±»Ba£ØOH£©2ČÜŅŗĪüŹÕ£»¢Ś¶žŃõ»ÆĢ¼ÓėĒāŃõ»Æ±µ·“Ӧɜ³ÉĢ¼Ėį±µÓėĖ®£¬·“Ó¦·½³ĢŹ½ĪŖCO2+Ba£ØOH£©2ØTBaCO3”ż+H2O£¬ĖłŅŌ“š°øŹĒ£ŗCO2+Ba£ØOH£©2ØTBaCO3”ż+H2O£»¢Ūa”¢ŌŚ¼ÓČėŃĪĖįÖ®Ē°£¬Ó¦Åž»×°ÖĆÄŚµÄCO2ĘųĢ壬·ĄÖ¹Ó°ĻģĢ¼Ėį±µÖŹĮæµÄ²ā¶Ø£¬æÉŅŌĢįøß²ā¶Ø×¼Č·¶Č£¬¹Źa²»·ūŗĻ£» b”¢µĪ¼ÓŃĪĖį¹żæģCO2 £¬ CO2Ą“²»¼°±»ĪüŹÕ£¬¾ĶÅųö×°ÖĆC£¬µĪ¼ÓŃĪĖį²»ŅĖ¹żæģ£¬Ź¹¶žŃõ»ÆĢ¼ĪüŹÕĶźČ«£¬æÉŅŌĢįøß²ā¶Ø×¼Č·¶Č£¬¹Źb²»·ūŗĻ£» c”¢ŌŚABÖ®¼äŌöĢķŹ¢ÓŠÅØĮņĖįµÄĻ“Ęų×°ÖĆ£¬ĪüŹÕĖ®·Ö£¬²»Ó°ĻģCO2 £¬ ²»ÄÜĢįøßĢįøß²ā¶Ø×¼Č·¶Č£¬¹Źc·ūŗĻ£» d”¢ŌŚBCÖ®¼äŌöĢķŹ¢ÓŠ±„ŗĶĢ¼ĖįĒāÄĘČÜŅŗµÄĻ“Ęų×°ÖĆBa£ØOH£©2 £¬ æÉŅŌĪüŹÕCO2ÖŠµÄHCl£¬Ó°ĻģCO2 £¬ ²»ÄÜĢįøß²ā¶Ø×¼Č·¶Č£¬¹Źd·ūŗĻ£®¹ŹŃ”£ŗcd£®¢ÜBaCO3ÖŹĮæĪŖ3.94g£¬Ōņn£ØBaCO3£©= ![]() =0.02mol£¬Ōņn£ØCaCO3£©=0.02mol£¬ÖŹĮæĪŖ0.02mol”Į100g/mol=2g£¬ĖłŅŌѳʷ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżĪŖ
=0.02mol£¬Ōņn£ØCaCO3£©=0.02mol£¬ÖŹĮæĪŖ0.02mol”Į100g/mol=2g£¬ĖłŅŌѳʷ֊Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżĪŖ ![]() ”Į100%=25%£¬ĖłŅŌ“š°øŹĒ£ŗ25%£»¢ŻBÖŠµÄĖ®ÕōĘų”¢ĀČ»ÆĒāĘųĢåµČ½ųČė×°ÖĆCÖŠ£¬µ¼ÖĀ²ā¶Ø¶žŃõ»ÆĢ¼µÄÖŹĮæĘ«“󣬲ā¶ØµÄĢ¼ĖįøʵÄÖŹĮæĘ«“ó£¬Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżĘ«øߣ¬ĖłŅŌ“š°øŹĒ£ŗBÖŠµÄĖ®ÕōĘų”¢ĀČ»ÆĒāĘųĢåµČ½ųČė×°ÖĆCÖŠ£®
”Į100%=25%£¬ĖłŅŌ“š°øŹĒ£ŗ25%£»¢ŻBÖŠµÄĖ®ÕōĘų”¢ĀČ»ÆĒāĘųĢåµČ½ųČė×°ÖĆCÖŠ£¬µ¼ÖĀ²ā¶Ø¶žŃõ»ÆĢ¼µÄÖŹĮæĘ«“󣬲ā¶ØµÄĢ¼ĖįøʵÄÖŹĮæĘ«“ó£¬Ģ¼ĖįøʵÄÖŹĮæ·ÖŹżĘ«øߣ¬ĖłŅŌ“š°øŹĒ£ŗBÖŠµÄĖ®ÕōĘų”¢ĀČ»ÆĒāĘųĢåµČ½ųČė×°ÖĆCÖŠ£®


 ŗ®¼ŁĄÖŌ°±±¾©½ĢÓż³ö°ęÉēĻµĮŠ“š°ø
ŗ®¼ŁĄÖŌ°±±¾©½ĢÓż³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶ¼Ļó·Ö±š±ķŹ¾ÓŠ¹Ų·“Ó¦µÄ·“Ó¦¹ż³ĢÓėÄÜĮæ±ä»ÆµÄ¹ŲĻµ£¬¾Ż“ĖÅŠ¶ĻĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©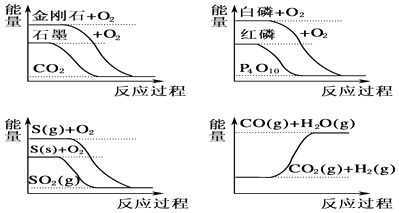
A.ŹÆÄ«×Ŗ±äĪŖ½šøÕŹÆŹĒĪüČČ·“Ó¦
B.°×Į×±ČŗģĮ×ĪȶØ
C.S£Øg£©+O2£Øg£©ØTSO2£Øg£©”÷H1 £¬ S£Øs£©+O2£Øg£©ØTSO2£Øg£©”÷H2 £¬ Ōņ”÷H1£¾”÷H2
D.CO£Øg£©+H2O£Øg£©ØTCO2£Øg£©+H2£Øg£©”÷H£¾0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ¶ĢÖÜĘŚŌŖĖŲµÄĖÄÖÖĄė×ÓA2£«”¢B£«”¢C3£”¢D£¾ßÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹,ŌņĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. Ō×ÓŠņŹż£ŗD£¾C£¾B£¾A B. Ō×Ó°ė¾¶£ŗB£¾A£¾C£¾D
C. Ąė×Ó°ė¾¶£ŗC3££¾D££¾A2£«£¾B£« D. Ńõ»ÆŠŌ£ŗA2£«£¾B£«£¬»¹ŌŠŌ£ŗC3££¼D£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬ŌŚVLĆܱÕČŻĘ÷ÖŠ£¬A”¢B”¢CČżÖÖĪļÖŹµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ÓÉĶ¼ÖŠŹż¾Ż·ÖĪö£ŗ 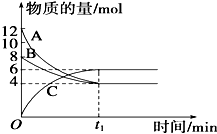
£Ø1£©·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø2£©“ÓæŖŹ¼µ½t1 minÄ©Ź±£¬ÓĆĪļÖŹC±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æFe(OH)3½ŗĢåĒų±šÓŚFeCl3ČÜŅŗ×ī±¾ÖŹµÄĢŲÕ÷ŹĒ (”” ””)
A. Fe(OH)3½ŗĢåĮ£×ӵēóŠ”ŌŚ1”«100 nmÖ®¼ä B. Fe(OH)3½ŗĢå¾ßÓŠ¶”“ļ¶ūŠ§Ó¦
C. Fe(OH)3½ŗĢåŹĒ¾łŅ»”¢ĪČ¶ØµÄ·ÖÉ¢Ļµ D. Fe(OH)3½ŗĢåµÄ·ÖÉ¢ÖŹÄÜĶø¹żĀĖÖ½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń.AŹĒŅ»ÖÖ³£¼ūµ„ÖŹ£¬A”¢B”¢C”¢DÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼£¬CŹĒŅ»ÖÖÄŃČÜŠŌĪļÖŹ”£
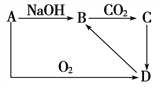
£Ø1£©ČōAŹĒŅ»ÖÖ½šŹō£¬ŌņAŹĒ________£¬ŹŌŠ“³öÓÉA”śB µÄĄė×Ó·½³ĢŹ½_________________________
£Ø2£©ČōAŹĒŅ»ÖÖ·Ē½šŹō£¬ŌņAŹĒ________£¬
ŹŌŠ“³öÓÉB”śC µÄĄė×Ó·½³ĢŹ½_______________________
¢ņ.ijĶ¬Ń§ŌŚ»Ä³ÖÖŌŖĖŲµÄŅ»ÖÖµ„ŗĖĪ¢Į£µÄ½į¹¹Ź¾ŅāĶ¼Ź±£¬Ķü¼ĒŌŚŌ²Č¦ÄŚ±ź³öĘäÖŹ×ÓŹż£¬ĒėÄćøł¾ŻĻĀĆęµÄĢįŹ¾×ö³ö×Ō¼ŗµÄÅŠ¶Ļ”£
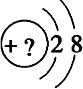
£Ø1£©øĆĪ¢Į£ŹĒÖŠŠŌĪ¢Į££¬ÕāÖÖĪ¢Į£µÄŌŖĖŲ·ūŗÅŹĒ____________
£Ø2£©øĆĪ¢Į£µÄ»¹ŌŠŌŗÜČõ£¬Ź§Č„1øöµē×Óŗó±äĪŖŌ×Ó£¬Ō×ÓµÄŃõ»ÆŠŌŗÜĒ棬øƵ„ÖŹÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½________________________________________
£Ø3£©øĆĪ¢Į£µÄŃõ»ÆŠŌŗÜČõ£¬µĆµ½1øöµē×Óŗó±äĪŖŌ×Ó£¬Ō×ӵĻ¹ŌŠŌŗÜĒ棬øƵ„ÖŹÓėŃõĘųČ¼ÉÕĖłµĆ²śĪļµÄµē×ÓŹ½______________
£Ø4£©øĆĪ¢Į£µÄ»¹ŌŠŌŗÜČõ£¬Ź§Č„2øöµē×Óŗó±ä³ÉŌ×Ó£¬ĘäĒā»ÆĪļµÄ½į¹¹Ź½______________
£Ø5£©øĆĪ¢Į£µÄ·ūŗÅĪŖX3+£¬ĘäĒāŃõ»ÆĪļÓėĒæ¼ī·“Ó¦µÄĄė×Ó·½³ĢŹ½____________________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
A. ĮņĖįµÄĦ¶ūÖŹĮæŹĒ98gB. 18gĖ®ÖŠŗ¬ÓŠĖ®·Ö×ÓŹżĪŖNA
C. O2µÄĦ¶ūÖŹĮæµČÓŚĘäĻą¶Ō·Ö×ÓÖŹĮæD. 1molCOµÄÖŹĮæĪŖ28g”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ16O”¢18O”¢H”¢T”¢DĪåÖÖŌ×Ó£¬æÉŅŌ¹¹³ÉĖ®·Ö×Ó£¬ĘäÖÖĄąÓŠ£Ø £©
A. 12B. 10C. 8D. 6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼¢ń”¢¢ņ·Ö±šŹĒ¼×”¢ŅŅĮ½×éĶ¬Ń§½«·“Ó¦”°AsO ![]() +2I©+2H+AsO
+2I©+2H+AsO ![]() +I2+H2O”±Éč¼Ę³ÉµÄŌµē³Ų×°ÖĆ£¬ĘäÖŠC1”¢C2¾łĪŖĢ¼°ō£®¼××éĻņĶ¼¢ńÉÕ±ÖŠÖšµĪ¼ÓČėŹŹĮæÅØŃĪĖį£»ŅŅ×éĻņĶ¼¢ņBÉÕ±ÖŠÖšµĪ¼ÓČėŹŹĮæ40%NaOHČÜŅŗ£®ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
+I2+H2O”±Éč¼Ę³ÉµÄŌµē³Ų×°ÖĆ£¬ĘäÖŠC1”¢C2¾łĪŖĢ¼°ō£®¼××éĻņĶ¼¢ńÉÕ±ÖŠÖšµĪ¼ÓČėŹŹĮæÅØŃĪĖį£»ŅŅ×éĻņĶ¼¢ņBÉÕ±ÖŠÖšµĪ¼ÓČėŹŹĮæ40%NaOHČÜŅŗ£®ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £© 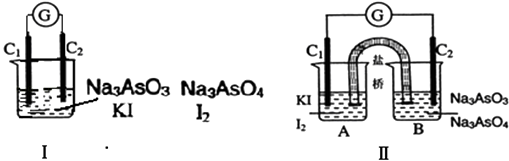
A.¼××é²Ł×÷Ź±£¬Ī¢°²±ķ
B.ÖøÕė·¢ÉśĘ«×Ŗ
C.¼××é²Ł×÷Ź±£¬ČÜŅŗŃÕÉ«±äÉī
D.ŅŅ×é²Ł×÷Ź±£¬C2×öÕż¼«
E.ŅŅ×é²Ł×÷Ź±£¬C1ÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖI2+2e©ØT2I©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com