
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂。回答下列问题:
(1)NOCl虽然不稳定,但其原子均达到8e-稳定结构,NOCl的电子式为_________________。
(2)一定条件下,在密闭容器中发生反应:2NOCl(g)![]() 2NO(g)+Cl2(g),其正反应速率表达式为v正=k·cn( NOCl)(k为速率常数),测得v正和c(NOCl)的关系如表:
2NO(g)+Cl2(g),其正反应速率表达式为v正=k·cn( NOCl)(k为速率常数),测得v正和c(NOCl)的关系如表:
序号 | c(NOCl)/(mol·L-1) | v正/(mol·L-1·s-1) |
① | 0.30 | 3.60×10-9 |
② | 0.60 | 1.44×10-8 |
则n=_________;k=___________。
(3)25 ℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
序号 | 热化学方程式 | 平衡常数 |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
则该温度下,ΔH3=______kJ/mol;K3=______(用K1和K2表示)。
(4)25℃时,在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图曲线a所示,则ΔH3=______(填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强(p)随时间(t)
的变化如图曲线b所示,则改变的条件是_____________;K3=___________L/mol;在5 min时,再充入0.08 mol NO和0.04 molCl2,则混合气体的平均相对分子质量将_____________(填“增大”、“减小”或“不变”)。

【答案】 ![]() 2 4×10-8 L/(mol·s) 2a-b
2 4×10-8 L/(mol·s) 2a-b ![]() < 加入催化剂 28.8 增大
< 加入催化剂 28.8 增大
【解析】(1)NOCl为共价化合物,氮、氧、氯三种原子间形成共价键,同时满足每个原子到8e-稳定结构,所以NOCl的电子式为![]() ;正确答案:
;正确答案:![]() 。
。
(2)根据v正=k·cn( NOCl)进行计算:①3.60×10-9= k·(0.30)n,②1.44×10-8= k·(0.60)n ,两式相除,得n=2;然后把n=2带入①式,3.60×10-9= k·(0.30)2, 得k=4×10-8 L/(mol·s);正确答案:2;4×10-8 L/(mol·s)。
(3)根据盖斯定律:①×2-②,得到反应③,因此:2NO(g)+Cl2(g)![]() 2NOCl(g) ΔH3=2a-b kJ/mol;①2NO2(g)+NaCl(s)
2NOCl(g) ΔH3=2a-b kJ/mol;①2NO2(g)+NaCl(s)![]() NaNO3(s)+NOCl(g) K1=c(NOCl)/c2(NO2);②4NO2(g)+2NaCl(s)
NaNO3(s)+NOCl(g) K1=c(NOCl)/c2(NO2);②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2=c2(NO)×c(Cl2)/c4(NO2);③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2=c2(NO)×c(Cl2)/c4(NO2);③2NO(g)+Cl2(g)![]() 2NOCl(g) K3= c2(NOCl)/c2(NO)×c(Cl2),所以K12/K2=K3;正确答案:2a-b;
2NOCl(g) K3= c2(NOCl)/c2(NO)×c(Cl2),所以K12/K2=K3;正确答案:2a-b; ![]() 。
。
(4)根据图像可知,正反应为气体物质的量减小的反应,但是开始时气体的压强增大,说明该反应为放热反应,ΔH3<0;若其他条件相同,改变某一条件后,气体的压强不变,说明平衡不移动,改变的条件只能为加入了催化剂;在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2,c(Cl2)=0.02mol/L,c(NO)= 0.04 mol/L,设消耗氯气的浓度为x mol/L,根据反应2NO(g)+Cl2(g)![]() 2NOCl(g)可知,反应达平衡后,剩余c(NO)=(0.04-2x)mol/L,c(Cl2)=(0.02-x)mol/L,生成c(NOCl)=2x mol/L;根据同一条件下,气体的压强之比等于气体的物质的量之比,因此平衡后气体的总浓度为(0.04-2x)+(0.02- x)+2x=(0.06-x)mol/L,反应前气体的总浓度为0.02+0.04=0.06 mol/L,0.06/(0.06-x)=8P1/7P1,解之得x=0.0075 mol/L,反应达平衡后K3=(0.015)2/(0.025)2×0.0125=28.8;反应在5 min时达到平衡,在此基础上,再充入0.08molNO和0.04molCl2,容器的体积不变,按比例增大反应物浓度,相当于加压的过程,平衡右移,气体总质量增大,气体总量减小,根据混合气体的平均相对分子质量=m(混)/n(混)可知,合气体的平均相对分子质量增大;正确答案:< ;加入催化剂;28.8; 增大。
2NOCl(g)可知,反应达平衡后,剩余c(NO)=(0.04-2x)mol/L,c(Cl2)=(0.02-x)mol/L,生成c(NOCl)=2x mol/L;根据同一条件下,气体的压强之比等于气体的物质的量之比,因此平衡后气体的总浓度为(0.04-2x)+(0.02- x)+2x=(0.06-x)mol/L,反应前气体的总浓度为0.02+0.04=0.06 mol/L,0.06/(0.06-x)=8P1/7P1,解之得x=0.0075 mol/L,反应达平衡后K3=(0.015)2/(0.025)2×0.0125=28.8;反应在5 min时达到平衡,在此基础上,再充入0.08molNO和0.04molCl2,容器的体积不变,按比例增大反应物浓度,相当于加压的过程,平衡右移,气体总质量增大,气体总量减小,根据混合气体的平均相对分子质量=m(混)/n(混)可知,合气体的平均相对分子质量增大;正确答案:< ;加入催化剂;28.8; 增大。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 15g乙烷分子中含有共价键的数目为3NA
B. 常温常压下,7g乙烯、丙烯的混合物含有原子数为1.5NA
C. 0.1mol/L的AlCl3溶液中含有的铝离子数为0.01NA
D. 25℃时,1L0.1mol/L的CH3COOH溶液中的H+数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)CO2的摩尔质量为_________,3.01×1023个CO2的质量为_________,在标准状况下其体积为_________;
(2)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸_________mL(保留两位有效数字);
(3)已知离子反应:RO3n﹣+6I﹣+6H+═R﹣+3I2+3H2O,推断:n=_________,R元素在RO3n﹣中的化合价是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学式中,正确的是( )
A. 甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2+3H2(g)![]() 2NH3(g);△H=-38.6kJ·mol-1
2NH3(g);△H=-38.6kJ·mol-1
C. 稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为:H+(aq)+OH-(aq)=H2O(1); △H=-57.3kJ·mol-1
D. 1molH2完全燃烧放热142.9kJ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1);△H=+285.8kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)可抑制金属腐蚀。以钼精矿(主要成分为MoS2,含少量杂质)为原料,制备钼酸钠晶体的主要流程图如下。

回答下列问题
(1)完成下列反应:_____MoS2+ _____O2![]() _____SO2+ _____MoO3
_____SO2+ _____MoO3
在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是__________________。
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为____________________________;该反应说明MoO3______(填“有”或“没有”)酸性氧化物的性质。
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则![]() =_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,
=_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,![]() 将_________(填“变大”“不变”或“变小”)。
将_________(填“变大”“不变”或“变小”)。
(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为_____________。
温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 |
析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | ||||||
溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45. |
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是_____________。
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是___________(填选项字母)。
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列几种有机物:
A.CH4 B.(CH3)2C=CHCH3 C.C2H2 D.C6H14 E.CH2=CHCH=CH2 F.环戊烷
请回答下列问题:[第(1)(3)问请用A、B、C等代码作答,第(4)问请用化学用语作答]
(1)上述有机物中互为同系物的是________,互为同分异构体的是________。
(2)请用系统命名法对B进行命名__________。
(3)发生加聚反应后的产物中具有单双键相间排列结构的单体是__________。
(4)CH4的质谱图上质荷比为16的微粒符号是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.液态氯化氢、固体氯化钾均不导电,故HCl和KCl均为非电解质
B.NH3、SO3水溶液都能导电,故二者均为电解质
C.铜和石墨均能导电,所以它们都是电解质
D.蔗糖、乙醇在水溶液中和熔融状态下都不导电,所以它们是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能用勒夏特列原理解释的是( )
A. 铁在潮湿的空气中易腐蚀
B. H2、I2、HI平衡混和气加压后颜色变深
C. 往往需要在催化剂条件下SO2氧化成SO3
D. 棕红色NO2加压后颜色先变深后变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是组成生物体的部分高分子化合物与组成它们的化学元素的关系图:
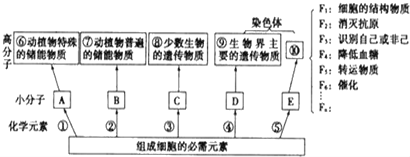
(1)构成小分子A、B、C、D、E的化学元素中,相同的元素有_____.
(2)写出下列高分子的名称:⑦___;⑨_____;⑩ _________.
(3)导致F1~Fn差别的原因是____________________________________.
(4)小分子C和D比较一定不同的是,前者含________,后者含______.
(5)写出下列物质的具体名称:F2为______;F6 为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com