

分析 (1)浓硫酸在乙醇的消去反应中作催化剂和脱水剂;浓硫酸具有强氧化性,则乙醇能够与浓硫酸发生副反应生成二氧化硫,二氧化硫能够使酸性高锰酸钾溶液褪色,所以需要先用碱液吸收;
(2)溴乙烷能够与氢氧化钠溶液发生反应生成乙醇,乙醇能够被酸性高锰酸钾溶液氧化,需要先用水除去;
(3)乙炔气体中混有硫化氢气体,可用硫酸铜溶液除去;碳化钙为离子化合物,阴阳离子需要标出所带电荷,阴离子还需要标出最外层电子;
(4)根据醇中含有氢键,氢键大于范德华力分析;
(5)丙三醇俗称甘油,丙三醇的结构简式为HOCH2CH2OH;乙二醇可由于制取汽车防冻液、化工原料等.
解答 解:(1)实验室利用乙醇能发生消去反应制乙烯:CH3-CH2-OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,在该反应中浓硫酸作催化剂、脱水剂;
乙醇能够与浓硫酸发生副反应生成二氧化硫,二氧化硫能够使酸性高锰酸钾溶液褪色,为了避免二氧化硫对检验乙烯的干扰,所以需要用NaOH溶液除去SO2,
故答案为:催化剂、脱水剂;NaOH;SO2能够使酸性高锰酸钾溶液褪色;
(2)溴乙烷与氢氧化钠溶液的反应中会发生副反应生成乙醇,乙醇能够使酸性高锰酸钾褪色,所以应该先用水吸收乙醇,目的是防止乙醇和酸性高锰酸钾反应,
故答案为:水;防止乙醇和酸性高锰酸钾反应;
(3)制取的乙炔气体中通常混有硫化氢气体,硫酸铜溶液能够与硫化氢反应,剩余实验室制乙炔时可用CuSO4溶液除杂质气体;碳化钙属于离子化合物,阴离子中存在碳碳三键,碳化钙的电子式为 ,
,
故答案为:CuSO4溶液; ;
;
(4)氢键的作用力大于范德华力,醇分子之间含有氢键,烷烃分子间含有范德华力,所以相对分子质量相近的醇比烷烃沸点高,
故答案为:醇分子之间含有氢键;
(3)丙三醇俗称甘油,分子中含有3个羟基,其结构简式为:CH2OH-CHOH-CH2OH;乙二醇可由于制取汽车防冻液、化工原料等,
故答案为:甘油;CH2OH-CHOH-CH2OH;汽车防冻液.
点评 本题考查了常见有机物制取方法及检验方法、物质的除杂方法等知识,题目难度不大,明确常见有机物的制取原理、检验方法为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
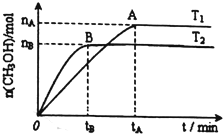 科学家利用太阳能分解水生产的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH).已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8kJ•mol-1、283.0kJ•mol-1和726.5kJ•mol-1.
科学家利用太阳能分解水生产的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH).已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8kJ•mol-1、283.0kJ•mol-1和726.5kJ•mol-1.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,5v正(O2)=4v逆(NO) | |
| B. | 若单位时间内生成nmol NO的同时,生成nmol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.7mol Na2O2与足量的CO2气体反应,电子转移0.7NA | |
| B. | 足量水蒸气与16.8gFe粉反应转移0.9mol电子 | |
| C. | Na与水、Al与NaOH溶液反应中水均作氧化剂 | |
| D. | 用钠从四氯化钛中置换钛,利用了钠的强还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①②③ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子的数目相等 | B. | 粒子的总的物质的量相等 | ||
| C. | 正电荷总数和负电荷总数应相等 | D. | 反应前后原子的数目不一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.0 | 342 |
| 硫酸钾 | 0.5 | 174 |
| 阿司匹林 | 0.4 | 180 |
| 高锰酸钾 | 0.5 | 158 |
| 硝酸银 | 0.2 | 170 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com