
科目:高中化学 来源: 题型:
| A、1 mol NaCl固体溶于1 L水所得溶液中NaCl的物质的量浓度为1 mol?L-1 |
| B、5.6 g铁在足量氯气中燃烧时失去的电子数目为0.3NA |
| C、常温常压下,11.2 L H2所含的分子数目为NA |
| D、17g氨气所含的质子数目为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用锌片作负极,铁片作正极,稀硫酸为电解质溶液一段时间后,溶液PH增大 |
| C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D、铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓海轮腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
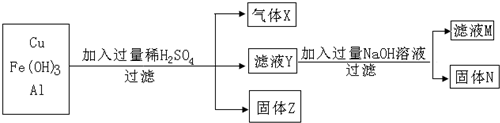
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 时间/mim | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 种类 | 1 | 2 | 3 | 4 | 5 |
| 组成化学式 |
| 55 |
| 28 |
| 组别 | Ⅰ | Ⅱ | Ⅲ |
| 盐酸的体积(ml) | 50 | 50 | 50 |
| A的质量(g) | 3.80 | 6.20 | 7.20 |
| 气体的体积(ml) | 896 | 1344 | 1344 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com