
现有如下仪器,仪器中已注入溶液,回答下列问题。
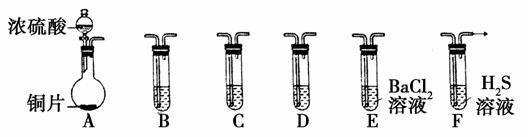
(1)加热装置A,写出铜与浓硫酸反应的化学方程式:_________,烧瓶中的实验现象为________________。
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________________、C________________、D________________。能说明碳的非金属性比硅强的实验现象是________________。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是_____________________,反应方程式为__________________________。
②若证明SO2具有还原性,在E中采取的实验操作为_________,其实验现象为________________,反应原理为________________(用离子方程式表示)。
解析:本题考查化学实验知识,意在考查考生分析问题和解决问题的能力。(1)浓硫酸具有强的氧化性,能与铜发生氧化还原反应,反应的化学方程式为Cu+2H2SO4(浓)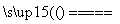 CuSO4+SO2↑+2H2O;烧瓶中的现象为:铜片变灰黑色,表面有气泡生成,烧瓶中可能有白色物质生成。(2)元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,要比较碳、硅的非金属性,可利用二氧化硫先制得二氧化碳,再将二氧化碳通入硅酸钠溶液中,若生成硅酸沉淀,则可证明碳的非金属性比硅强,为排除二氧化硫的干扰,应在通入二氧化碳前,用KMnO4溶液除去二氧化硫,若KMnO4溶液不褪色,说明二氧化硫被除尽,硅酸钠溶液中出现白色沉淀,说明有硅酸生成。故B可以是Na2CO3溶液或NaHCO3溶液,C为KMnO4溶液,D为Na2SiO3溶液。(3)①二氧化硫和氯化钡溶液不反应,当H2S溶液中有浅黄色浑浊出现时即可证明二氧化硫有氧化性,其反应方程式为2H2S+SO2===3S↓+2H2O。②将氯气通入E装置的BaCl2溶液中,若有白色沉淀生成,则证明二氧化硫具有还原性,其离子方程式为Ba2++SO2+Cl2+2H2O===BaSO4↓+4H++2Cl-。
CuSO4+SO2↑+2H2O;烧瓶中的现象为:铜片变灰黑色,表面有气泡生成,烧瓶中可能有白色物质生成。(2)元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,要比较碳、硅的非金属性,可利用二氧化硫先制得二氧化碳,再将二氧化碳通入硅酸钠溶液中,若生成硅酸沉淀,则可证明碳的非金属性比硅强,为排除二氧化硫的干扰,应在通入二氧化碳前,用KMnO4溶液除去二氧化硫,若KMnO4溶液不褪色,说明二氧化硫被除尽,硅酸钠溶液中出现白色沉淀,说明有硅酸生成。故B可以是Na2CO3溶液或NaHCO3溶液,C为KMnO4溶液,D为Na2SiO3溶液。(3)①二氧化硫和氯化钡溶液不反应,当H2S溶液中有浅黄色浑浊出现时即可证明二氧化硫有氧化性,其反应方程式为2H2S+SO2===3S↓+2H2O。②将氯气通入E装置的BaCl2溶液中,若有白色沉淀生成,则证明二氧化硫具有还原性,其离子方程式为Ba2++SO2+Cl2+2H2O===BaSO4↓+4H++2Cl-。
答案:(1) Cu+2H2SO4(浓)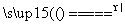 CuSO4+SO2↑+2H2O(1分) 铜片变灰黑色,表面有气泡生成,烧瓶中可能有白色物质生成(2分)
CuSO4+SO2↑+2H2O(1分) 铜片变灰黑色,表面有气泡生成,烧瓶中可能有白色物质生成(2分)
(2)Na2CO3溶液或NaHCO3溶液(合理即可,1分)KMnO4溶液(1分)Na2SiO3溶液(1分)C中KMnO4溶液不褪色,D中出现白色沉淀(1分)
(3)①H2S溶液中有浅黄色浑浊出现(1分)2H2S+SO2===3S↓+2H2O(1分)②通入氯气(或加入氯水或加入过氧化氢溶液或加入高锰酸钾溶液等)(其他合理答案均可,1分)有白色沉淀生成(1分) Ba2++SO2+Cl2+2H2O===BaSO4↓+4H++2Cl-(根据所加入试剂写出离子方程式,2分)


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下图所示的实验装置或操作不能达到实验目的的是( )
|
|
|
|
|
| A.实验室制取氨气 | B.配制100 mL 0.1 mol/L盐酸 | C.测定中和反应的反应热 | D.实验室制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含如下离子组中的若干种:K+、Fe3+、Fe2+、Cl-、CO 、NO
、NO 、SO
、SO 、SiO
、SiO 、I-,某同学欲探究该溶液的组成,进行如下实验:
、I-,某同学欲探究该溶液的组成,进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰。
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成。
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
A.原溶液中肯定不含Fe2+、NO 、SiO
、SiO 、I-
、I-
B.步骤Ⅱ中无色气体是NO气体,无CO2气体产生
C.原溶液中肯定含有K+、Fe3+、Fe2+、NO 、SO
、SO
D.为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
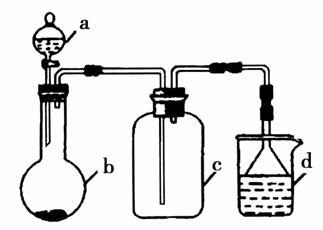
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
| C | 浓硝酸 | Cu | NO2 | H2O |
| D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
三氯化磷(PCl3)是一种重要的半导体材料掺杂剂。实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示。
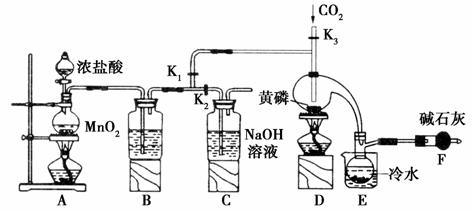
已知:PCl3遇O2会生成POCl3,POCl3能溶于PCl3,且PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
请回答下列问题:
(1)A中制氯气的离子方程式为________________。
(2)B中所装试剂是________________。
(3)E中冷水的作用是________________。
(4)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通入干燥CO2的作用是________________。
(5)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过________________(填实验操作名称),即可得到较纯净的PCl3。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一不可变容器中发生如下反应:2NO2  2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
2NO + O2 ΔH >0 达到平衡后,升温,混合气体的( )不变
A. 密度 B.颜色 C.压强 D. 总物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
|
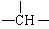 CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是 A.苹果酸中能发生酯化反应的官能团有2种
B.1mol苹果酸可与3mol NaOH发生中和反应
C.1mol苹果酸与足量金属Na反应生成生成1mol H2
D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com