
| A、pH=1的溶液中:K+、AlO2-、SO42-、NH4+ |
| B、饱和氯水中:Cl-、NO3-、Na+、SO32- |
| C、能使pH试纸变红的溶液:NH4+、Na+、SO42-、Fe2+ |
| D、AlCl3溶液中:K+、Na+、SO42-、HCO3- |


科目:高中化学 来源: 题型:
| A、HNO2非常不稳定,其分解产物为NO和H2O |
| B、NO2与水的反应机理:NO2先与水发生岐化反应生成HNO2和HNO3,HNO2再分解 |
| C、HNO2的酸性强于碳酸的酸性 |
| D、NO2通入NaOH溶液中,生成的HNO2和HNO3都与NaOH发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相对分子质量相同的有机物是同分异构体 |
| B、烷烃分子中,相邻的三个碳原子有可能在同一条直线上 |
| C、每个碳原子的化合价都已“饱和”,碳原子之间只以单键相结合的链烃一定是烷烃 |
| D、分子组成上相差一个或若干个CH2原子团的物质,互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾水解的离子方程式:Al3++3H2O?Al(OH)3+3H+ |
| B、CaCO3(s)=CaO(s)+CO2(g)△S>0 |
| C、用纯碱溶液洗涤餐具的原因,用离子方程式表示:CO32-+2H2O?H2CO3+2OH- |
| D、BaSO4悬浊液中存在平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、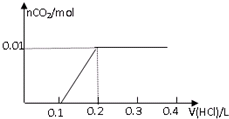 |
B、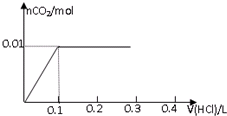 |
C、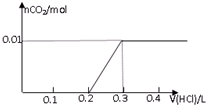 |
D、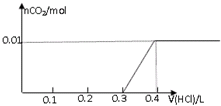 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、② | B、① | C、③ | D、①、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加压时(容器体积减小),正反速率增大 |
| B、保持压强不变,加入N2,正反速率变小 |
| C、保持压强不变,加入少许N2O4,再达到平衡,颜色变深 |
| D、保持体积不变,升高温度,再达到平衡时,颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
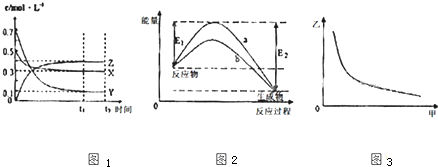
| A、该反应的化学方程式为X(g)+3Y(g)?2Z(g) |
| B、若图Ⅲ中甲表示压强,乙表示Z的含量,则其变化符合图Ⅲ中曲线 |
| C、该温度下,反应的平衡常数数值约为533.若升高温度,该反应的平衡常数减小,Y的转化率降低 |
| D、图II中曲线a、b可表示使用不同催化剂的能量变化曲线 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com