
已知有如下反应:①2BrO3-+Cl2==Br2+2ClO3-,②ClO3-+5Cl-+6H+==3Cl2+3H2O,
③2FeCl3+2KI==2FeCl2+2KCl+I2,④2FeCl2+Cl2==2FeCl3。下列各微粒氧化能力由强到弱的顺序正确的是 ( )
A. ClO3->BrO3->Cl2>Fe3+>I2 B. BrO3->Cl2>ClO3->I2>Fe3+
C. BrO3->ClO3->Cl2>Fe3+>I2 D. BrO3->ClO3->Fe3+>Cl2>I2
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述不正确的是
A.常温常压下,16g14CH4所含中子数目为8NA B.1 mol -CH3含有9 NA个电子
C.常温常压下,44 g CO2气体含有氧原子的个数为2 NA
D.46gNO2和N2O4的混合物含有的原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3
 溶液。加入KIO3和析出I2的物质的量的关系曲线如下图
溶液。加入KIO3和析出I2的物质的量的关系曲线如下图
所示。下列说法不正确的是
A.0~b间反应:3HSO3-+ IO3-= 3SO42-+ I-+ 3H+
B.a点时消耗NaHSO3的物质的量为1.2 mol
C.b~c间反应:I2仅是氧化产物
D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的
KIO3 为1.08mol
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯
化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe3+、Br2哪个氧化性更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生氧化还原反应所致,则
溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述现象是发生氧化还原反应所致,则溶液呈黄色是含
所致。
(3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实
验现象,证明了乙同学的观点是正确的。
供选用的试剂:a、酚酞试液 b、CCl4 c、无水酒精 d、KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到得现象。
| 选用试剂(填序号) | 实验现象 | |
| 方案1 | ||
| 方案2 |
(4)结论
氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生
的离子反应方程式为 。
(5)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是 。
②在100mLFeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应判断有关物质还原性由强到弱的顺序是 ( )
H2SO3+I2+H2O==2HI+H2SO4 2FeCl3+2HI==2FeCl2+2HCl+I2
3FeCl2+4HNO3==2FeCl3+NO↑+2H2O+Fe(NO3)3
A. H2SO3>I->Fe2+>NO B. I->Fe2+>H2SO3>NO
C. Fe2+>I->H2SO3>NO D. NO>Fe2+>H2SO3>I-
查看答案和解析>>
科目:高中化学 来源: 题型:
水作为还原剂的反应是 ( )
A. 2Na+2H2O==2NaOH+H2↑ B. SO3+H2O==H2SO4 C. 2F2+2H2O=4HF+O2 D. 2H2+O2 2H2O
2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是Br2+Na2CO3+H2O  NaBr + NaBrO3+NaHCO3,吸收1mol Br2时,转移的电子数为 mol。
NaBr + NaBrO3+NaHCO3,吸收1mol Br2时,转移的电子数为 mol。
(3)海水提镁的一段工艺流程如下图:
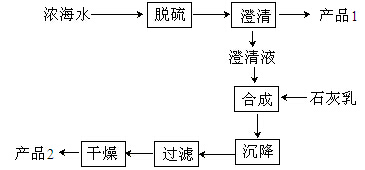
浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为 ,1L浓海水最多可得到产品2的质量为 g。
(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com