
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是

A. 电池工作时,光能转变为电能,X为电池的正极
B. 镀铂导电玻璃的作用是传递I-
C. 电解质溶液中发生反应:2Ru3++3I-=2Ru2++I3-
D. 电池的电解质溶液中I-和I3-的浓度均不断减小
【答案】C
【解析】由图中电子的移动方向可知,电极X为原电池的负极,发生氧化反应,电极反应为:2Ru2+-2e-=2Ru3+,Y 电极为原电池的正极,电解质为I-和I3-的混合物,I3-在正极上得电子被还原,正极反应为I3-+2e-=3I-。A、电池工作时,光能转变为电能,由图电子的移动方向可知,电极X为原电池的负极,选项A错误;B、电池工作时,电极为原电池的正极,发生还原反应,则镀铂导电玻璃的作用是作正极材料,选项B错误;C、电池工作时,负极反应为2Ru2+-2e-=2Ru3+,正极反应为I3-+2e-=3I-,又Ru2+和Ru3+,I3-和I-相互转化,所以电解质溶液中发生反应,选项C正确;D、由电池中发生的反应可知,I3-在正极上得电子被还原为I-,后又被氧化为I3-,I3-和I-相互转化,反应的实质是光敏有机物在激发态与基态的相互转化,所有化学物质都没有被损耗,选项D错误。答案选C。


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案科目:高中化学 来源: 题型:
【题目】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
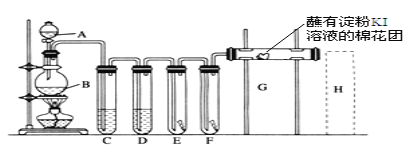
(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式_____________。
(2)D中放入浓H2SO4,其目的是_____________________________。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________,对比E和F中现象的差异可得出的结论及解释是________________________________。
(4)G处的现象是____________________________________。
(5)画出H处尾气吸收装置图并注明试剂____________。
(6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式__________。
②需“密闭保存”的原因____________________________________________。
(7)现在有一种名为“净水丸”的产品也能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。亚硫酸钠将水中多余次氯酸除去的离子反应方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )

![]()
A. 用图1所示装置从KI和I2的固体混合物中回收I2
B. 用图2所示装置配制100 mL 0.10 mol·L-1 K2Cr2O7溶液
C. 用图3所示装置干燥少量的SO2气体
D. 用图4所示装置蒸干FeCl3饱和溶液制备FeCl3晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭燃烧时产生大量SO2、NO对坏境影响极大。
(1)使用清洁能源可有效减少SO2等的排放。煤的液化是现代能源工业中重点推广的能源综合利用方案,最常见的液化方法为用煤生产CH3OH。已知制备甲醇的有关化学反应及平衡常数如下:
i:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-90.8kJ/mol
CH3OH(g)+H2O(g) △H1=-90.8kJ/mol
ii:C0(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41.2kJ/mol
CO2(g)+H2(g) △H2=-41.2kJ/mol
iii:CO(g)+2H2(g)![]() CH3OH(g) △H3
CH3OH(g) △H3
850℃时,三个反应的平衡常数分别为K1=160、K2=243、K3=160。甲醇还可以与乙酸反应制香料,反应为:CH3OH(l)+CH3COOH(l)![]() CH3COOCH3(l)+H2O(l)
CH3COOCH3(l)+H2O(l)
①△H3=_______制香料反应的平衡常数K 的表达式为____________。
②850℃时,在密闭容器中进行反应i,开始时只加入CO2、H2,反应10min后测得各组分的浓度如下表。比较正、逆反应的速率的大小:V正_____V逆 (填“>”、“<”或“=”)。
物质 | H2 | CO2 | CH3OH | H2O |
浓度/mol/L | 0.2 | 0.2 | 0.4 | 0.4 |
(2)研究人员发现,将煤炭在O2/CO2的气氛下燃烧,能够降低然煤时NO的排放,主要反应为:2NO(g)+2CO(g)=N2(g)+2CO2(g)。在一定温度下,于2L的恒容密闭容器中充入0.1molNO和0.3molCO发生该反应,如图为容器内的压强(p)与起始压强(p0)的比值(p/p0)随时间的变化曲线。
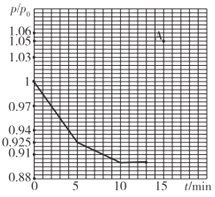
①0~5min内,该反应的平均反应速率V(N2)=______;平衡时NO的转化率为________。
②若13min时,向该容器中再充入0.06molCO,15min时再次达到平衡,此时容器内p/p0的比值应在图中A点的______(填"上方”或“方”)。
(3)以连二硫酸盐(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO),装置如图所示:

①阴极区的电极反应式为_________。
②NO吸收转化后的主要产物为NH4+,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为_______mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在通常条件下能一步转化的全部组合是
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ①②③ B. ①③④ C. ②③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
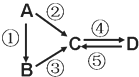
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列事实得出的结论正确的是
A. 试样![]() 产生银镜 结论:该试样是醛类
产生银镜 结论:该试样是醛类
B. 某卤代烃试样![]() 最终的沉淀不是白色;结论:该卤代烃中不含氯原子
最终的沉淀不是白色;结论:该卤代烃中不含氯原子
C. 往淀粉溶液中加入稀硫酸并且加热一段时间,再加入新制的氢氧化铜悬蚀液再加热。发现没有红色沉淀生成;结论: 淀粉没有水解生成葡萄糖
D. 将溴乙烷和NaOH的醇溶液混合加热,得到的气体先通入水中再通入酸性KMnO4溶液,溶溶褪色,说明发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是
A.一定条件下石墨转化为金刚石反应吸热说明石墨比金刚石稳定
B.化学反应必然伴随发生能量变化
C.化学键是一种作用力
D.不同元素组成的多原子分子中的化学键一定是极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,CuSO4(s)和 CuSO4·5H2O(s)溶于水及CuSO4·5H2O受热分解的能量变化如图所示,下列说法不正确的是
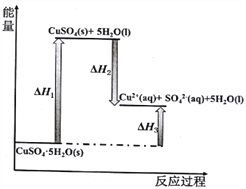
A. 将CuSO4·5H2O(s)溶于水会使溶液温度降低
B. 将CuSO4(s)溶于水会使溶液温度升高
C. △H3>△H2
D. △H1=△H2+△H3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com