
【题目】铁及其化合物之间的相互转化可用下式表示:![]()
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4 . 若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是 (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为﹣2价)则下列说法正确的是 (选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式: FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3 . 高铁酸钾作为水处理剂发挥的作用是 、 .
【答案】d;d;2;6;2;2;2;1;净水;消毒
【解析】(1)要使产物纯净,必须物质间发生反应后,没有杂质生成.
a、氯气有氧化性,能氧化二价铁离子生成三价铁离子,但同时有氯离子生成,所以有杂质生成,故a错误;
b、铁与稀硫酸反应生成二价铁离子,不能把二价铁离子转化为三价铁离子,故b错误;
c、硝酸能氧化二价铁离子生成三价铁离子,但溶液中还有杂质硝酸根离子,故c错误;
d、双氧水能氧化二价铁离子生成三价铁离子,同时有水生成,水是原溶液的成分,所以不是杂质,故d正确;
故选d;
(2)a、合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,所以黄铜矿不是合金,故a错误;
b、CuFeS2中铁元素的化合价为+2价,反应物Fe3+的化合价为+3价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,故b错误;
c、CuFeS2中只有S元素的化合价只有升高,其他元素的化合价不变,所以CuFeS2只作还原剂,故c错误;
d、CuFeS2+4Fe3+=Cu2++5Fe2++2S 转移电子4
184g 4mol
46g 1mol
故d正确;
故选d;
(3)FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,该反应,FeSO4中Fe的化合价为+2价,K2FeO4中Fe的化合价为+6价,所以一个氯化亚铁分子失去4个电子;K2O2中O的化合价为﹣1价,O2中O的化合价为0价,一个K2O2分子失去2个电子生成氧气;K2O2中O的化合价为﹣1价,K2FeO4和K2O中O元素的化合价为﹣2价,所以一个K2O2失去2个电子,该方程式中得失电子的最小公倍数为6,所以该方程式的计量数分别为2、6、2、2、2、1,即方程式为2FeSO4+6K2O2=2K2FeO4+2K2O+2K2SO4+1O2↑,
所以答案是:2、6、2、2、2、1;
(4)高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒,所以答案是:净水;消毒.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】超细碳酸钙的应用非常广泛。下图为工业生产超细碳酸钙的流程图:

(1)反应池中发生反应的化学方程式为___________。
(2)将反应池中得到的固体过滤、洗涤、烘干,得到超细碳酸钙。判断固体是否洗净的操作是__________。
(3)实验小组在实验室中利用如图所示装置(部分夹持装置已略去)模拟侯氏制碱法制纯碱。

实验步骤:
I.食盐精制:粗盐(含少量Ca2+、Mg2+、SO32-)溶解,依次加入足量NaOH溶液、______溶液、_______溶液;过滤;加入盐酸调pH至7。
II.转化:①将精制后的食盐溶液控制温度在30~35℃之间;不断搅拌,先后通入足量氨气和二氧化碳气体;保温,搅拌半小时;
②静置,过滤、洗涤、烘干,得到NaHCO3晶体。
III.制纯碱:将制得的NaHCO3放入坩埚中,在酒精灯上灼烧,冷却至室温,即得到纯碱。
已知各物质在不同温度下的溶解度见右表。
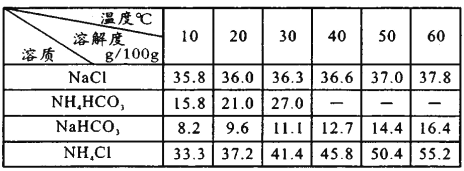
①B中应盛装________。
②C装置中发生“转化”生成NaHCO3的离子方程式是___________。
③“转化”过程中,温度控制在30~35℃之间的加热方式是_______;温度需控制在30~35℃之间的原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下A、B、C的如图所示的转化关系,且△H=△H1+△H2 . 则A、C可能是( ) 
①Fe、FeCl3
②C、CO2
③AlCl3、NaAlO2
④NaOH、NaHCO3
⑤S、SO3
⑥Na2CO3、CO2 .
A.②③④⑥
B.②③④⑤⑥
C.①②③④⑥
D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气通入石灰乳制得漂白粉,其主要成分是Ca(OH)2·3CaCl( ClO)·H2O。已知次氯酸盐可与盐酸反应生成氯气,用贮存过久的漂白粉与浓盐酸制得的Cl2中,含量最多的杂质气体除水蒸气外,还可能是
A. HC1,O2 B. CO2,HCl C. HC1 ,H2 D. CO2,H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入(或通入)Y溶液中,其生成沉淀的量与加入X的物质的量的关系如下图所示,符合图示情况的是( )
| A | B | C | D |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10.00mL 0.01mol/L某一元酸HA溶液中逐滴加入0.01mol/L NaOH 溶液,溶液pH变化曲线如图示.下列说法不正确的是( ) 
A.HA是弱酸
B.b点表示的溶液中:2c(Na+)=c(A﹣)+c(HA)
C.c点时:V=10.00mL
D.b、c、d点表示的溶液中:c(Na+)+c(H+)=c(A﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表所示:
实验编号 | HA物质的量浓度(mol*L﹣1) | NaOH物质的量浓度(mol*L﹣1) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)从①组情况表明,HA是(填“强酸”或“弱酸”).
(2)②组情况表明,c0.2(选填“大于”、“小于”或“等于”).混合液中离子浓度c(A﹣)与c(Na+)的大小关系是 .
(3)从③组实验结果分析,说明HA的电离程度NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是 .
(4)①组实验所得混合溶液中由水电离出的c(OH﹣)与溶液中的c(OH﹣)之比为 . 写出该混合溶液中下列算式的精确结果(不能近似计算):c(Na+)﹣c(A﹣)=molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用单质铜制硝酸铜,耗用原料最经济,而且对环境几乎没有污染的是( )
A.Cu ![]() Cu(NO3)2
Cu(NO3)2
B.Cu ![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
C.Cu ![]() Cu(NO3)2
Cu(NO3)2
D.Cu ![]() CuCl2
CuCl2 ![]() Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )
A.Na+、Fe3+、NO3﹣、Cl2都可在该物质的溶液中大量共存
B.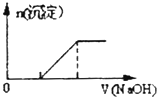
向O.1mo1﹣L﹣1该物质的溶液中清加0.Lmol﹣1NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示
C.检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D.向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com