
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
根据下列实验事实得出的相应结论正确的是( )
序号 | 实验事实 | 结论 |
A | 气体A的水溶液可以导电 | A不一定是电解质 |
B | 向某溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成 | 原溶液中含SO42- |
C | 向某溶液中滴加CCl4,振荡、静置,下层溶液呈紫红色 | 原溶液中一定有I- |
D | 某钠盐加入盐酸,若有气体生成 | 该盐一定是碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二12月月考化学卷(解析版) 题型:选择题
下列对有机反应类型的描述不正确的是( )
A.甲苯使酸性KMnO4溶液褪色,是因为发生了氧化反应
B.将苯加入溴水中,振荡后水层接近无色,是因为发生了取代反应
C.乙烯使溴的四氯化碳溶液褪色,是因为发生了加成反应
D.甲烷与氯气混合,光照一段时间后黄绿色消失,是因为发生了取代反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一12月月考化学试卷(解析版) 题型:选择题
用NaOH固体配制一定物质的量浓度的溶液200 mL,需经过称量、溶解、转移、定容等操作。下列图示对应的操作规范的是
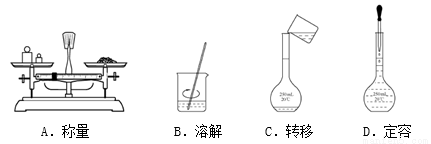
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一12月月考化学试卷(解析版) 题型:选择题
下列物质中,既能与盐酸又能与NaOH溶液反应的是
A.碳酸钠 B.硅酸钠 C.氢氧化铝 D.二氧化硅
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:填空题
部分弱酸的电离平衡常数如表。
弱酸 | HCOOH | H2S | H2SO3 |
电离平衡常数 (25℃) | K=1.8×10-4 | K1=9.1×10-8 K2=1.1×10-12 | K1=1.23×1 K2=6.6×10-8 |
(1)物质的量均为0.1mol/L的溶液①HCO ONa②NaHS③Na2SO3,pH最大的是________(填编号)
ONa②NaHS③Na2SO3,pH最大的是________(填编号)
(2)设计实验证明HCOOH为弱酸
(3)室温下,下列溶液中水电离出的c(H+)水由大到小的顺序为________(填编号)
①pH=12的NaOH溶液 ②NaCl溶液 ③pH=6的NH4Cl溶液 ④0.01mol/L醋酸
(4)二元酸H2A在水中存在以下电离:H2A=H++HA-,HA- H++A2-,试回答下列问题:
H++A2-,试回答下列问题:
①NaHA溶液呈 (填“酸性”、“碱性”、“中性” )
②某温度下,10mL、0.1mol/LNaHA溶液中加入0.1mol/LKOH溶液VmL至中性,此时溶液中以下关系一定正确的是(  )
)
A.溶液的pH=7 B.Kw=c2(OH-) C.V=10 D.c(K+)< c(Na+)
(5)如图横坐标为室温下溶液的pH,纵坐标为金属离子物质的量浓度的对数(当溶液中金属离子浓度≤10-5mol/L时,可认为沉淀完全)。试回答:
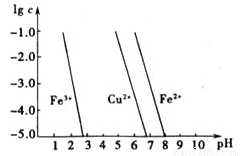
腐蚀铜板的溶液中,若Cu2+、Fe3+、Fe2+浓度均为0.1mol/L,向混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为 。
从图中的数据计算可得Fe(OH)2溶度积Ksp[Fe(OH)2]= 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:选择题
室温下,pH均为2的两种一元酸HA和HB各1mL,分别加水稀释,pH随溶液体积的变化曲线如下图所示。下列说法正确的是( )
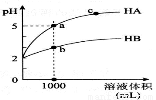
A.HA的酸性比HB的酸性弱
B.a点溶液的导电性比c点溶液的导电性弱
C.若两溶液无限稀释,则它们的c(H+)相等
D.对a、b两点溶液同时升高温度,则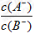 增大
增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:推断题
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D是海水中浓度最高的盐(部分反应物和生成物及水已略去)。
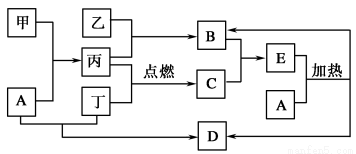
请回答下列问题:
(1)写出乙与丙生成B的反应条件:________________。
(2)写出甲和A溶液反应的离子方程式:______________。
(3)检验E中的阳离子时,取少量E于试管中, 则证明E中有该阳离子。
(4)写出实验室制取B的化学方程式:________________。
(5)B常见用途:_______________、_______________、_______________。
(6)常用作工业制某酸的原料,写出由B制该酸过程中的化学方程式:
______________________、 、________________。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上月考三化学试卷(解析版) 题型:实验题
亚硝酸钠是重要食品添加剂。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)查阅资料:①HNO2为弱酸,室温下存在反应:3HNO2=HNO3+2NO↑+H2O;
②NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
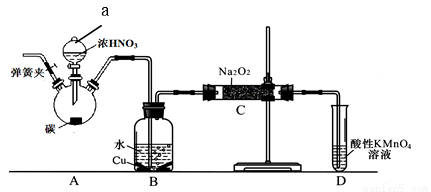
实验操作:
①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠。
回答下列问题:
(1)装置中仪器a的名称为 ,A中反应的化学方程式是 ;
(2)D装置的作用是 ;
(3)C中反应生成NaNO2的化学方程式是 ;
(4)检验C中产物有亚硝酸钠的正确操作是 (填序号) ;
a.取少量生成物溶于稀硫酸,若产生无色气体并在液体上方变为红棕色,则含有NaNO2
b.取少量生成物溶于水充分振荡,滴加酚酞试液,若溶液变红,则含有NaNO2
(5)经检验C的产物中亚硝酸钠含量较少。
①甲同学认为C中产物不仅有亚硝酸钠,还可能有其它固体物质。为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂应是 (写名称);
②乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com