
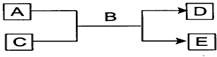
·ÖĪö A”¢B”¢C”¢D”¢E¾łĪŖ֊ѧ»Æѧ³£¼ūµÄ“æ¾»Īļ£¬BĪŖ×ŌČ»½ēÖŠŗ¬Įæ×ī¶ąµÄŅŗĢ壬ŌņBĪŖH2O£®
£Ø1£©³£ĪĀĻĀ£¬ČōAĪŖĘųĢ¬µ„ÖŹ£¬CĪŖ·Ē½šŹōŃõ»ÆĪļ£¬A”¢C¾łÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬Ļą¶Ō·Ö×ÓÖŹĮæE£¾D£¬ŌņAĪŖCl2£¬CĪŖSO2£¬EĪŖH2SO4£¬DĪŖHCl£»
£Ø2£©ČōAĪŖ¶ĢÖÜĘŚµÄ½šŹōµ„ÖŹ£¬DĪŖĘųĢ¬µ„ÖŹ£¬CČÜŅŗ³ŹĖįŠŌ»ņĒæ¼īŠŌŹ±£¬øĆ·“Ó¦¶¼ÄܽųŠŠ£¬ŌņAĪŖAl£¬DĪŖH2£»
£Ø3£©ČōA”¢C¾łĪŖ»ÆŗĻĪļ£¬CĪŖŅżĘšĪĀŹŅŠ§Ó¦µÄÖ÷ŅŖĘųĢ壬Ŋ¶ĻCĪŖCO2£¬ĪŖĖįŠŌĒæµÄÖʱøĖįŠŌČõµÄ·“Ó¦£¬EĪŖ°×É«³Įµķ£¬ÅŠ¶ĻEĪŖAl£ØOH£©3»ņH2SiO3£¬ŌņAĪŖĘ«ĀĮĖįŃĪ”¢¹čĖįŃĪ£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢E¾łĪŖ֊ѧ»Æѧ³£¼ūµÄ“æ¾»Īļ£¬BĪŖ×ŌČ»½ēÖŠŗ¬Įæ×ī¶ąµÄŅŗĢ壬Ŋ¶ĻĪŖH2O£»
£Ø1£©³£ĪĀĻĀ£¬ČōAĪŖĘųĢ¬µ„ÖŹ£¬CĪŖ·Ē½šŹōŃõ»ÆĪļ£¬A”¢C¾łÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬Ļą¶Ō·Ö×ÓÖŹĮæE£¾D£¬ŌņAĪŖCl2£¬CĪŖSO2£¬EĪŖH2SO4£¬DĪŖHCl£¬Ōņ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSO2+Cl2+2H2OØT2HCl+H2SO4£¬¼ģŃéDÖŠŅõĄė×ÓĖłÓĆŹŌ¼ĮĪŖ£ŗAgNO3 ČÜŅŗ£¬Ļ”HNO3£¬
¹Ź“š°øĪŖ£ŗSO2+Cl2+2H2OØT2HCl+H2SO4£»AgNO3 ČÜŅŗ£¬Ļ”HNO3£»
£Ø2£©ČōAĪŖ¶ĢÖÜĘŚµÄ½šŹōµ„ÖŹ£¬DĪŖĘųĢ¬µ„ÖŹ£¬CČÜŅŗ³ŹĖįŠŌ»ņĒæ¼īŠŌŹ±£¬øĆ·“Ó¦¶¼ÄܽųŠŠ£¬ŌņAĪŖAl£¬DĪŖH2£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Al+2OH-+2H2O=2AlO2-+3H2”ü£¬
¹Ź“š°øĪŖ£ŗ2Al+2OH-+2H2O=2AlO2-+3H2”ü£»
£Ø3£©ČōA”¢C¾łĪŖ»ÆŗĻĪļ£¬CĪŖŅżĘšĪĀŹŅŠ§Ó¦µÄÖ÷ŅŖĘųĢ壬Ŋ¶ĻCĪŖCO2£¬ĪŖĖįŠŌĒæµÄÖʱøĖįŠŌČõµÄ·“Ó¦£¬EĪŖ°×É«³Įµķ£¬ÅŠ¶ĻEĪŖAl£ØOH£©3»ņH2SiO3£¬ŌņAĪŖĘ«ĀĮĖįŃĪ”¢¹čĖįŃĪ£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3£»H2SiO3£»
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļĶʶĻ£¬Ö÷ŅŖæ¼²éĀČĘų”¢Įņ¼°Ęä»ÆŗĻĪļ”¢ĀĮ¼°Ęä»ÆŗĻĪļµČĪļÖŹŠŌÖŹµÄĶʶĻŗĶŌĖÓĆ£¬ŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬ĢāÄæÄѶČÖŠµČ


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
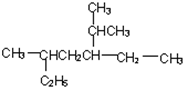
| A£® | 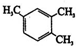 1£¬3£¬4-Čż¼×»ł±½ | B£® | 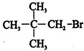 2-¼×»łĀȱūĶé | C£® |  2-¶”“¼ | D£® |  2-¼×»ł-3-¶”Č² |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā

| A£® | øĆ·“Ó¦æÉÄÜĪŖæÉÄę·“Ó¦ | |
| B£® | øĆ·“Ó¦æɱķŹ¾ĪŖ2AB2?2AB3 | |
| C£® | µ„Ī»Ź±¼äÄŚÉś³É1 mol B2µÄĶ¬Ź±Éś³É2 mol AB2£¬Õā±ķĆ÷øĆ·“Ó¦ŅŃ“ļĘ½ŗā | |
| D£® | øĆ¹ż³ĢÖŠ£¬ŅŃ·“Ó¦µÄAB2Õ¼AB2×ÜŹżµÄ$\frac{2}{3}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĖłÓŠĀ±“śĢž¶¼ŹĒÄŃČÜÓŚĖ®”¢ĆܶȱČĖ®Š”µÄŅŗĢå | |
| B£® | ĖłÓŠĀ±“śĢžŌŚ³£ĪĀĻĀ¶¼ŹĒŅŗĢ壬ĒŅ¶¼ŹĒ·Ēµē½āÖŹ | |
| C£® | ĖłÓŠĀ±“śĢž¶¼ŗ¬ÓŠĀ±Ō×Ó | |
| D£® | ĖłÓŠĀ±“śĢž¶¼ŹĒĶعżČ”“ś·“Ó¦ÖĘµĆµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 2£¬5-¶ž¼×»ł-3-ŅŅ»ł-øżĶé
2£¬5-¶ž¼×»ł-3-ŅŅ»ł-øżĶé +3H2$\stackrel{“߻ƼĮ}{”ś}$
+3H2$\stackrel{“߻ƼĮ}{”ś}$ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
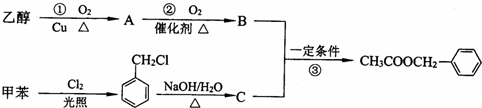
 £®
£® £®£®
£®£® ”¢
”¢ £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com