
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E¾łĪŖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£ĘäÖŠAŌŖĖŲŌ×ÓŗĖÄŚÖ»ÓŠŅ»øöÖŹ×Ó£»AÓėC”¢BÓėD·Ö±šĶ¬Ö÷×壻B”¢DĮ½ŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶŹĒA”¢CĮ½ŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶµÄ2±¶”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÓÉÉĻŹöŌŖĖŲ×é³ÉµÄĻĀĮŠĪļÖŹÖŠŹōÓŚ·Ēµē½āÖŹµÄŹĒ________(Ģī×ÖÄø)”£
A£®C2B2 B£®DB2 C£®E2 D£®C2DB3
£Ø2£©DŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ_______________________________£»»ÆŗĻĪļC2BÖŠĮ½ÖÖĄė×ӵİė¾¶“󊔹ŲĻµĪŖ________£¾________(ĢīĄė×Ó·ūŗÅ)”£
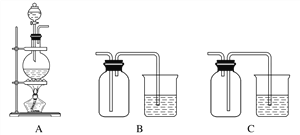
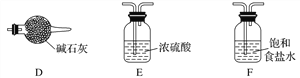
£Ø3£©ŹµŃéŹŅÖŠÓūŃ”ÓĆĻĀĮŠ×°ÖĆÖĘČ”²¢ŹÕ¼Æ“æ¾»øÉŌļµÄE2ĘųĢ唣ŹµŃé֊ӦєÓƵÄ×°ÖĆĪŖ________________(°“ÓÉ×óµ½ÓŅµÄĮ¬½ÓĖ³ŠņĢīŠ“)£»
”¾“š°ø”æ B µŚČżÖÜĘŚ¢öA×å O2£ Na£« AFEB
”¾½āĪö”æAŌŖĖŲŌ×ÓŗĖÄŚÖ»ÓŠ1øöÖŹ×Ó£¬ŌņAĪŖHŌŖĖŲ£¬AÓėCĶ¬Ö÷×壬ŌņCĪŖNaŌŖĖŲ£¬BÓėDĶ¬Ö÷×壻B”¢DĮ½ŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶŹĒA”¢CĮ½ŌŖĖŲŌ×ÓŠņŹżÖ®ŗĶµÄ2±¶£¬ŌņB”¢D·Ö±šĪŖO”¢SŌŖĖŲ£¬A”¢B”¢C”¢D”¢E¾łĪŖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ŌņEĪŖClŌŖĖŲ”£
£Ø1£©A£®C2B2ĪŖ¹żŃõ»ÆÄĘ£¬ŹĒµē½āÖŹ£¬A“ķĪó£»B£®DB2 ĪŖSO2£¬ŹōÓŚ·Ēµē½āÖŹ£¬BÕżČ·£»C£®E2ŹĒĀČĘų£¬²»ŹĒµē½āÖŹ£¬Ņ²²»ŹĒ·Ēµē½āÖŹ£¬C“ķĪó£»D£®C2DB3ĪŖNa2SO3£¬ŹōÓŚµē½āÖŹ£¬D“ķĪ󣬓š°øŃ”B”££Ø2£©DŌŖĖŲĪŖS£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠĪ»ÓŚµŚ3ÖÜĘŚ¢öA×壻»ÆŗĻĪļC2BĪŖNa2O£¬ŗ¬ÓŠµÄĮ½ÖÖĄė×ÓĪŖNa+”¢O2£¬µē×ÓÅŲ¼ĻąĶ¬£¬Ō×ÓŠņŹżŌ½“ó£¬Ąė×Ó°ė¾¶Ō½Š”£¬ĖłŅŌO2°ė¾¶“óÓŚNa+°ė¾¶£»£Ø3£©ŹµŃéŹŅÓĆMnO2ÓėÅØŃĪĖį¼ÓČČÖĘČ”Cl2£¬·¢Éś×°ÖĆĪŖA£¬ÖĘČ”µÄCl2ÖŠŗ¬ÓŠHClŗĶĖ®·Ö£¬ĖłŅŌĮ¬½ÓF³żČ„HCl£¬ŌŁĮ¬½ÓE³żČ„Ė®·Ö£¬×īŗóĮ¬½ÓB£¬ŹÕ¼ÆCl2²¢“¦ĄķĪ²Ęų£¬¹ŹŃ”ÓƵÄ×°ÖĆŅĄ“ĪĪŖAFEB”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĆčŹöÖŠÕżČ·µÄŹĒ£Ø £©
A.ClO2©µÄæռ乹ŠĶĪŖĘ½ĆęČż½ĒŠĪ
B.SiF4ŗĶSO32©µÄÖŠŠÄŌ×Ó¾łĪŖsp3ŌÓ»Æ
C.ŌŚĖłÓŠµÄŌŖĖŲÖŠ£¬·śµÄµŚŅ»µēĄėÄÜ×ī“ó
D.C2H5OH·Ö×ÓÖŠ¹²ŗ¬ÓŠ8øö¼«ŠŌ¼ü£¬1øö¦Š¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·śŌŚ×ŌČ»½ēÖŠ³£ŅŌCaF2µÄŠĪŹ½“ęŌŚ£®
£Ø1£©ĻĀĮŠ¹ŲÓŚCaF2µÄ±ķŹöÕżČ·µÄŹĒ £®
a£®Ca2+ÓėF©¼ä½ö“ęŌŚ¾²µēĪüŅż×÷ÓĆ
b£®F©µÄĄė×Ó°ė¾¶Š”ÓŚCl© £¬ ŌņCaF2µÄČŪµćøßÓŚCaCl2
c£®ŅõŃōĄė×Ó±ČĪŖ2£ŗ1µÄĪļÖŹ£¬¾łÓėCaF2¾§Ģå¹¹ŠĶĻąĶ¬
d£®CaF2ÖŠµÄ»Æѧ¼üĪŖĄė×Ó¼ü£¬Ņņ“ĖCaF2ŌŚČŪȌדĢ¬ĻĀÄܵ¼µē
£Ø2£©CaF2ÄŃČÜÓŚĖ®£¬µ«æÉČÜÓŚŗ¬Al3+µÄČÜŅŗÖŠ£¬ŌŅņŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£©£®
ŅŃÖŖAlF63©ŌŚČÜŅŗÖŠæÉĪČ¶Ø“ęŌŚ£®
£Ø3£©F2ĶØČėĻ”NaOHČÜŅŗÖŠæÉÉś³ÉOF2 £¬ OF2·Ö×Ó¹¹ŠĶĪŖ £¬ ĘäÖŠŃõŌ×ÓµÄŌӻƷ½Ź½ĪŖ
£Ø4£©F2ÓėĘäĖūĀ±ĖŲµ„ÖŹ·“Ó¦æÉŅŌŠĪ³ÉĀ±ĖŲ»„»ÆĪļ£¬ĄżČēClF3”¢BrF3µČ£®ŅŃÖŖ·“Ó¦Cl2£Øg£©+3F2£Øg£©ØT2ClF3£Øg£©”÷H=©313kJmol©1 £¬ F©F¼üµÄ¼üÄÜĪŖ159kJmol©1 £¬ Cl©Cl¼üµÄ¼üÄÜĪŖ242kJmol©1 £¬ ŌņClF3ÖŠCl©F¼üµÄĘ½¾ł¼üÄÜĪŖkJmol©1 £® ClF3µÄČŪ”¢·Šµć±ČBrF3µÄ£ØĢī”°øß”±»ņ”°µĶ”±£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ÖŠµÄB”«K·Ö±š“ś±ķÓŠ¹Ų·“Ó¦µÄŅ»ÖÖ·“Ó¦Īļ»ņÉś³ÉĪļ£¬ĘäÖŠA”¢C”¢F”¢KŹĒ¹ĢĢ壻EŹĒ³£¼ūµÄĘųĢåµ„ÖŹ£®¹ĢĢ¬ĪļÖŹA¼ÓČČŗóÉś³ÉµÄĘųĢå»ģŗĻĪļČōĶعż¼īŹÆ»ŅÖ»Ź£ÓąĘųĢåB£¬ČōĶعżÅØĮņĖįŌņÖ»Ź£ÓąĘųĢåD£®ø÷ĪļÖŹ¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ŗ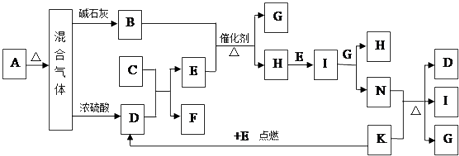
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öŹµŃéŹŅ¼ģŃéAĪļÖŹÖŠŗ¬ÓŠµÄŃōĄė×ӵķ½·Ø
£Ø2£©BÓėE·“Ó¦µĆµ½1molH£¬Ōņ“ĖŹ±×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖmol£®
£Ø3£©Š“³öŹµŃéŹŅÖĘČ”BµÄ»Æѧ·½³ĢŹ½ £®
£Ø4£©Š“³öNµÄĻ”ČÜŅŗÓė¹żĮæµÄĢś·Ū·“Ó¦µÄĄė×Ó·½³ĢŹ½ £®
£Ø5£©Čō»ģŗĻĘųĢåĶعż¼īŹÆ»ŅµĆµ½µÄĘųĢåBÓėĶعżÅØĮņĖįµĆµ½µÄĘųĢåDµÄĪļÖŹµÄĮæÖ®±ČŹĒ8£ŗ5£¬ŌņÓĆĪļÖŹµÄĮæµÄ¹ŲĻµ±ķŹ¾“Ė¹ĢĢåAµÄ×é³ÉĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒ²æ·Ö¶ĢÖÜĘŚŌŖĖŲŌ×Ó°ė¾¶ÓėŌ×ÓŠņŹżµÄ¹ŲĻµĶ¼”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
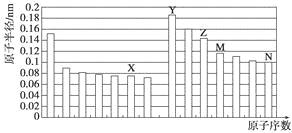
A. Z”¢NĮ½ÖÖŌŖĖŲµÄĄė×Ó°ė¾¶Ļą±Č£¬Ē°Õß½Ļ“ó
B. X”¢NĮ½ÖÖŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļµÄ·ŠµćĻą±Č£¬Ē°Õß½ĻµĶ
C. ÓÉXÓėMĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ²»ÄÜÓėČĪŗĪĖį·“Ó¦£¬µ«ÄÜÓėĒæ¼ī·“Ó¦
D. ZµÄŃõ»ÆĪļÄÜ·Ö±šČܽāÓŚYµÄĒāŃõ»ÆĪļŗĶNµÄĒā»ÆĪļµÄĖ®ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŅĒĘ÷æÉŅŌ¼ÓČȵďĒ£Ø £©
¢ŁÕōĮóÉÕĘ棻¢ŚČŻĮæĘ棻¢ŪÕō·¢Ćó£»¢ÜŹŌ¹Ü£»¢Ż±ķĆęĆ󣻢Ž·ÖŅŗĀ©¶·£»¢ßĮæĶ²£»¢ą×¶ŠĪĘæ
A. ¢Ł¢Ū¢Ü¢ąB. ¢Ś¢Ü¢Ž¢ąC. ¢Ū¢Ü¢ŻD. ¢Ś¢Ū¢Ü¢ß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŅĒĘ÷£ŗ¢ŁÉÕ±£»¢Ś×¶ŠĪĘ棻¢ŪŌ²µ×ÉÕĘ棻¢ÜŹŌ¹Ü£»¢ŻŪįŪö£»ĘäÖŠæÉŅŌÓĆ¾Ę¾«µĘÖ±½Ó¼ÓČȵÄŅĒĘ÷ŹĒ£Ø””””£©
A. ¢Ł¢Ś¢Ū¢Ü B. ¢Ü¢Ż C. ¢Ł¢Ū D. ¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ飬²¢»Ų“šĻĀĮŠĪŹĢā£ŗ 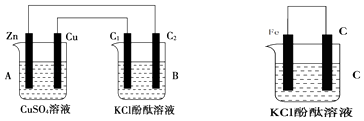
£Ø1£©ÅŠ¶Ļ×°ÖƵÄĆū³Ę£ŗA³ŲĪŖ £¬ B³ŲĪŖ £®
£Ø2£©Šæ¼«ĪŖ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£»ŹÆÄ«°ōC1ĪŖ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£»ŹÆÄ«°ōC2ø½½ü·¢ÉśµÄŹµŃéĻÖĻóĪŖ £®
£Ø3£©Š“³öC ×°ÖĆÖŠČÜŅŗŃÕÉ«±äŗģµÄµē¼«·“Ó¦Ź½£ŗ £®
£Ø4£©µ±C2¼«Īö³ö224mLĘųĢå£Ø±ź×¼×“æöĻĀ£©Ź±£¬CuSO4ČÜŅŗµÄÖŹĮæ±ä»ÆĮĖg£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠČēĻĀ»Æѧ·“Ó¦£ŗCO2£Øg£©+H2£Øg£©CO£Øg£©+H2O£Øg£©£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKŗĶĪĀ¶ČtµÄ¹ŲĻµČēĻĀ±ķ£ŗ
t”ę | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ
£Ø2£©·“Ó¦ŹĒ·“Ó¦£®£ØŃ”Ģī”°ĪüČČ”±”¢·ÅČČ£©£®
£Ø3£©ÄÜÅŠ¶ĻøĆ·“Ó¦ŹĒ·ń“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ £®
a£®ČŻĘ÷ÖŠŃ¹Ēæ²»±ä b£®»ģŗĻĘųĢåÖŠc£ØCO£©²»±ä
c£®vÕż£ØH2£©=vÄę£ØH2O£© d£®c£ØCO2£©=c£ØCO£©
£Ø4£©Ä³ĪĀ¶ČĻĀ£¬Ę½ŗāÅØ¶Č·ūŗĻĻĀŹ½£ŗc£ØCO2£©c£ØCH2£©=c£ØCO£©c£ØH2O£©£¬ŹŌÅŠ¶Ļ“ĖŹ±µÄĪĀ¶ČĪŖ”ę
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com