
【题目】工业上可由乙苯(C8H10)生产苯乙烯(C8H8),其反应原理是:![]() 下列说法中错误的是
下列说法中错误的是
A. 可用溴的四氯化碳来鉴别乙苯和苯乙烯
B. 乙苯分子中所有原子可能都处于同一平面
C. 苯乙烯可发生氧化反应、取代反应、加成反应
D. 乙苯与苯互为同系物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列
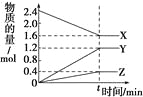
表述中正确的是
A. 反应的化学方程式为2X = 3Y + Z
B. t时,正、逆反应都不再继续进行,反应达到化学平衡
C. 若t=4,则0~t的X的化学反应速率为0.1 molL-1min-1
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷元素生产和生活中有广泛的应用。
(1)P原子价电子排布图为____。
(2)四(三苯基磷)钯分子结构如图1。
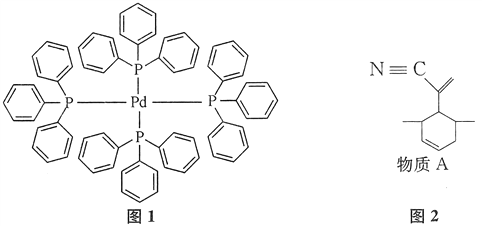
P原子以正四面体的形态围绕在钯原子中心上,判断该物质在水中溶解度并加以解释:_________。该物质可用于图2所示物质A的合成,物质A中碳原子杂化轨道类型为____;一个A分子中手性碳原子数目为____。
(3)在图3中表示出四(三苯基磷)钯分子中配位键____。
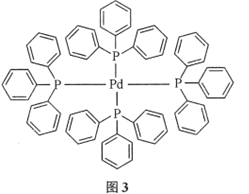
(4)PCl5是一种白色晶体,在恒容密闭容器中加热可在148℃液化,形成一种能导电的熔体,测得其中含有一种正四面体形阳离子和一种正六面体形阴离子,熔体中P-Cl的键长只有198nm和206nm两种,这两种离子的化学式为____;正四面体形阳离子中键角大于PCl3的键角原因为_____。
(5)磷有三种含氧酸H3PO2、H3PO3、H3PO4,其中磷元素均以sp3杂化与相邻原子形成四个σ键,则H3PO3的结构式是________,写出H3PO2与足量氢氧化钠溶液反应的化学方程式:____________________。磷的三种含氧酸H3PO2、H3PO3、H3PO4的酸性强弱顺序为H3PO2<H3PO3<H3PO4,其原因是_____________________。
(6)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。
①写出合成磷化硼的化学反应方程式:____________________
②三溴化硼分子和三溴化磷分子的立体构型分别是________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的种类繁多,但其命名中是有规则的。下列有机物命名正确的是
A.CH3(CH2)4CH3 1,4二甲基丁烷
B.CH3CH(CH3)CH=CH2 甲基丁烯
C.CH3CH2CH(CH3) CH2OH 2甲基1丁醇
D.CH2ClCH2Cl 二氯乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.卤代烃是一类重要的有机合成中间体,是许多有机合成的原料。根据卤代烃的相关性质,回答下列问题
(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如右图所示,则A的结构简式为___________,

请预测B的核磁共振氢谱上应该有__________个峰(信号)。
(2)某同学用如图1装置(铁架台、酒精灯等略)验证取代反应和消去反应的产物。
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH水溶液和0.5 mL溴乙烷振荡。
实验操作Ⅱ:将试管如图1固定后,水浴加热。
①据图1:用水浴加热而不直接用酒精灯加热的原因是_________________。

②图2是为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,
实验中需要检验的产物是_________________________,
水的作用是________________________________________,
实验现象是___________________________________________。
Ⅱ.下图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热装置、铁架台、铁夹等均未画出)。图中:A、无水乙醇(沸点:78.5℃),B、绕成螺旋状的细铜丝或银丝,C、无水硫酸铜粉末,D、碱石灰,E、高锰酸钾,F、蒸馏水
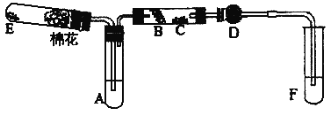
(1)为使A中乙醇平稳转化成乙醇蒸汽,常采用的方法是_________________;
(2)D处碱石灰的作用______________________;
(3)反应后的C处实验现象是: _____________ ;
(4)写出B处发生反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
现将A进行如下图所示反应,已知:D的相对分子质量比E小,B不能发生银镜反应,F可使溴水褪色,且其中含甲基。
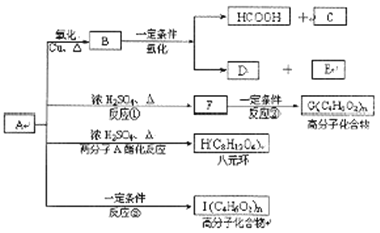
试回答下列问题:
(1)写出下列物质的结构简式:A_______C_______D_______。
(2)反应①②③的反应类型:①______②______③________
(3)写出下列变化的化学方程式:
① E与邻笨二胺(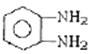 )缩聚生成一种合成纤维:_________;
)缩聚生成一种合成纤维:_________;
② F→G______________;
③ A→H______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )

A. 溶液中OH-向电极a移动
B. 反应消耗的NH3与O2的物质的量之比为4:3
C. 负极的电极反应式为2NH3-6e-+6OH-=N2+6H2O
D. 电子迁移方向:电极a→导线→电极b→电解质溶液→电极a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质不属于同分异构体的是( )
A. 2,2﹣二甲基丙醇和2﹣甲基丁醇 B. 甲基丙烯酸和甲酸丙酯
C. 2﹣甲基丁烷和戊烷 D. 邻氯甲苯和对氯甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气代替石油生产液体燃料和基础化学品是当前化学研究和发展的重点。
(1)我国科学家创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产乙烯、芳香烃Y和芳香烃Z等重要化工原料,实现了CO2的零排放,碳原子利用率达100%。已知Y、Z的相对分子质量分别为78、128,其一氯代物分别有1种和2种。
①有关化学键键能数据如表中所示:
化学键 | H-H | C=C | C-C | C≡C | C-H |
E(kJ/mol) | 436 | 615 | 347.7 | 812 | 413.4 |
写出甲烷一步生成乙烯的热化学方程式_________________________,反应中硅化物晶格限域的单中心铁催化剂的作用是________________________;
②已知:原子利用率=期望产物总质量/反应物总质量×100%,则甲烷生成芳香烃Y的原子利用率为___________;
③生成1 mol Z产生的H2约合标准状况下________L。
(2)如图为乙烯气相直接水合法制备乙醇中乙烯的平衡转化率与温度、压强的关系
(其中n(H2O):n(C2H4)=1:1)。
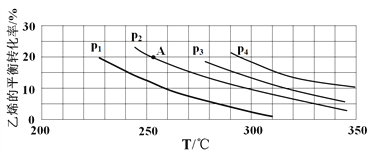
①若p2=8.0 MPa,列式计算A点的平衡常数Kp=____________(用平衡分压代替平衡浓度计算;分压=总压×物质的量分数;结果保留到小数点后两位);
②该反应为__________(填“吸热”或“放热”)反应,图中压强(p1、p2、p3、p4)的大小关系为____________,理由是________________;
③气相直接水合法常采用的工艺条件:磷酸/硅藻土为催化剂,反应温度为290℃,压强为6.9 MPa,n(H2O):n(C2H4)=0.6:1。乙烯的转化率为5%,若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有______________(任写两条)。
(3)乙烯可以作为燃料电池的负极燃料,请写出以熔融碳酸盐作为电解质时,负极的电极反应式________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com