
| A、燃烧反应都属于放热反应 |
| B、化学反应必然伴随着能量的变化 |
| C、吸热反应是指需要加热才能进行的反应 |
| D、化学键的断裂和形成是化学反应中能量变化的主要原因 |


科目:高中化学 来源: 题型:
| A、卤素单质与水反应均可用X2+H2O=HXO+HX表示 |
| B、HX都极易溶于水,它们的热稳定性随X的核电荷数的增加而减小 |
| C、卤素单质的颜色由F2→I2按相对分子质量增大而变深 |
| D、X-的还原性依次为:F-<Cl-<Br-<I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
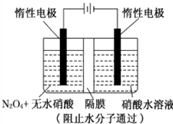 如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )
如图所示装置可通过发生“3N2O4+8HNO3=6N2O5+2NO+4H2O”制备N2O5,有关说法中错误的是( )| A、阴极的电极反应为:NO3-+4H++3e-=NO↑+2H2O |
| B、阳极的电极反应为:N2O4+2 HNO3-2e-=2N2O5+2H+ |
| C、当电路中通过6 mol e-时整个电解池中参与反应的HNO3为8mol |
| D、当电路中通过6 mol e-时,有8molH+从阳极向阴极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是( )
在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是( )| A、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| C、在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D、在D点:c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B、自发反应在恰当条件下才能实现 |
| C、自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| D、自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入溴水振荡,观察水层是否有棕红色出现 |
| B、滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无白色沉淀生成 |
| C、加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无白色沉淀生成 |
| D、加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸、碱和盐类都属于电解质,其他化合物都是非电解质 |
| B、强电解质与弱电解质的本质区别,是其水溶液导电性的减弱 |
| C、电解质与非电解质的本质区别,是在水溶液或熔化状态下能否电离 |
| D、常见的强酸、强碱和大部分盐都是强电解质,其他化合 物都是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl溶液在电流作用下电离成Na+与Cl- |
| B、溶于水后能电离出H+的化合物都是酸 |
| C、液态氯化氢不能导电,但氯化氢是电解质 |
| D、导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com